恒瑞、石药攻超10亿品种 第一个国产脂质体来了
近日,恒瑞、石药先后申请伊立替康脂质体上市,原研发产品今年4月刚刚获批进入国内市场。伊立替康是一个超过10亿的抗肿瘤品种。恒瑞早就有一定的市场地位,石药作为国内脂质体龙头企业,也有优势。
图1:伊立替康脂质体相关产品最近申报上市
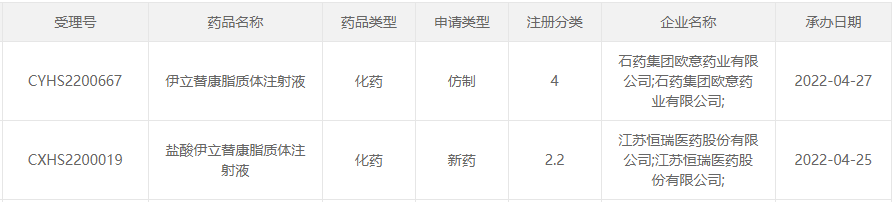
来源:CDE官网
图2:伊立替康近年来的销售情况(单位:亿元)
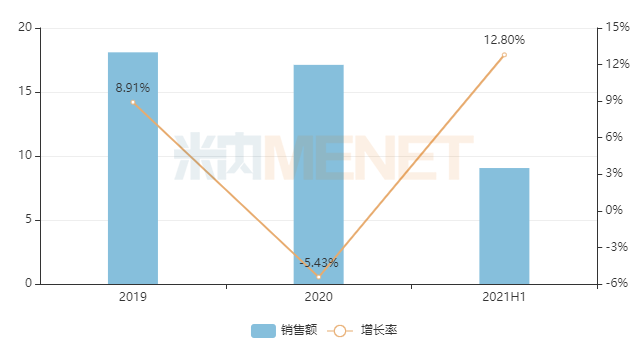
来源:中国公立医疗机构终端竞争格局
米内网数据显示,目前国内市场上畅销的伊立替康制剂包括盐酸伊立替康注射液和注射盐酸伊立替康。2020年,两大产品在中国城市公立医院、县级公立医院、城市社区中心和乡镇卫生院(以下简称中国公立医疗机构)终端销售规模超过17亿元,2021年上半年增速高达12.80%。
恒瑞已获得盐酸伊立替康注射液和盐酸伊立替康注射生产批准,2021年上半年占全国总量的一半。
2022年4月,原研制的盐酸伊立替康脂质体注射液获批进入国内市场,适应症为和谐。5-氟尿嘧啶(5-FU)和亚叶酸(LV)转移性胰腺癌患者联合用于吉西他滨治疗。
早在2018年,石药就首次申请了伊立替康脂质体注射液三类仿制上市,最终获批临床实践。这一次,它被列为四类仿制品;恒瑞盐酸伊立替康脂质体注射液按2.2新药申报上市。
图3:石药伊立替康脂质体注射液临床情况

来源:米内网新版数据库
伊立替康脂质体注射液对晚期胆道癌、晚期胰腺癌、小细胞肺癌、乳腺癌等适应症进行了相关临床试验,其中胰腺癌生物等效性试验于2021年1月完成。
图4:恒瑞盐酸伊立替康脂质体注射液临床情况

来源:米内网新版数据库
恒瑞医药在公告中提到,提交上市申请的盐酸伊立替康脂质体注射适应症是联合5-FU/LV吉西他滨治疗失败后,二线治疗局部晚期或转移性胰腺癌。数据显示,恒瑞还对食管癌、一线晚期胰腺癌等适应症进行了相关临床试验,总研发费用约1亿元。
此外,南京绿叶制药、四川科伦药物研究院、江苏奥赛康药业、齐鲁药业也获得了盐酸伊立替康脂质体注射液的临床批准。可以预见,未来一段时间,高端制剂的市场竞争将加剧。
