上市仅一年 美敦力全球首款被一级召回
4月26日,FDA宣布将美敦力Harmony经导管肺动脉瓣(TPV)导管系统列为I召回级别,即最严重的召回级别,是指设备可能造成严重伤害或死亡。
Harmony经导管肺动脉瓣(TPV)该系统是世界上第一个自膨胀肺动脉瓣,曾被用作世界上第一个自膨胀肺动脉瓣FDA被认定为突破性设备,加速了其审批。2021年3月,该设备获得了该设备的批准。FDA批准。
但获批仅一年,2022年3月2日,美敦力立即启动了对Harmony经导管肺动脉瓣(TPV)2021年4月7日至2022年1月26日,在美国分发的665台设备受到召回事件的影响。
到目前为止,已经报告了六起临床病例的投诉,共有一起受伤和零死亡与设备使用有关。
01
设备有断裂的风险
将暂停使用
肺动脉瓣置换术(Transcatheter pulmonary valve replacement,TPVR)最初于2000年开始治疗右室流出道重建后并发右室流出道功能不全(包括狭窄和回流)的患者,就像治疗右室流出道重建后并发右室流出道功能不全的患者一样TAVR同样,微创植入可以延缓开放式手术,改善此类患者的长期预后。
TPVR虽然最早出现,但受患者数量、适应证、耐久性和推广价值的影响,发展相对较大TAVR相对滞后。
Harmony经导管肺动脉瓣(TPV)这是世界上第一款自膨胀肺动脉瓣,之前上市的TPVR产品主要为球囊扩张瓣膜,如美敦力Melody和爱德华的Sapien。
球囊扩张瓣膜型号小,不适合长期使用PR肿瘤扩张RVOT解剖学的特点进一步导致了解剖学的特点TPVR使用量有限。
Harmony获批不仅解决了球囊扩张瓣膜型号小的问题,还让美敦力实现了TPVR对于爱德华的领先地位,后者的产品仍在临床研究中。
但这一全球首款获批仅一年,2022年3月2日,美敦力即将对抗Harmony导管输送系统发起召回的原因是放置TPV在此过程中,将胶囊固定在输送导管末端的粘结可能会断裂。
断裂可能导致手术延迟,或需要额外安排。一旦手术过程中断裂,可能会对患者造成严重伤害。这些风险包括:防止血流和/或完全阻塞(栓塞或闭塞)、撕裂和/或分裂(穿孔或夹层)或其他类型的血管损伤。
召回产品批次
据报道,有6起来自临床病例的投诉,一起受伤,没有与使用这些设备相关的死亡。
FDA根据相关召回页面,受召回事件影响的是2021年 4月 7日至 2022年 1月 26日在美国分发的665台设备。
受影响的是:
1.计划将 Harmony TPV 植入严重肺动脉瓣反流患者的医务人员
2.使用 Harmony TPV 系统瓣膜置换的候选人
美敦力还特别指出,召回只适用于召回Harmony TPV输送导管,而不是Harmony TPV。已成功植入Harmony TPV患者,无需采取任何行动。
20224月6日,美敦力向植入医生和客户发出紧急医疗器械召回通知,建议立即暂停使用Harmony TPV输送导管。
客户须知包括:
1.将导管从所有未使用的产品中移除并退回美敦力。
2.暂停Harmony TPV系统新植入病例。
3.要求客户填写附有信函的表格,以确认收到召回并报告未使用的设备数量。
查阅了FDA目前共有1483个 相关页面Harmony TPV该系统已在美国和加拿大分发,目前尚不清楚召回是否会扩展到所有产品以及在加拿大销售的部分。
02
美敦力陷I级召回门
中国受到了很大的影响
近两年来,美敦力频频陷入困境I召回事件,让人分不清是旧闻还是新闻。
支架断裂致死,糖尿病业务重挫
根据FDA2021年,美敦力10次召回被归类为数据库I级。
其中Valiant Navion胸支架移植系统发生了极为罕见的临床事故支架断裂Valiant Evo支架在全球临床试验中断裂,其中纤维管撕裂,血液泄漏到主动脉,导致一名受试者死亡。
而MiniMed胰岛素泵是美敦力糖尿病业务的核心产品,其召回也给美敦力带来了很大的麻烦。
MiniMed 670G
202110月10日,美敦力扩大召回MiniMed 508、Paradigm泵的遥控器,和MiniMed 600系列泵,两次召回均属于I召回有严重伤害或死亡的风险。召回严重影响了美敦力的糖尿病业务。
20212012年12月,美敦力收到FDA警告信被命名为胰岛素泵和遥控器召回问题处理不力。为了解决相关问题,美敦力新胰岛素泵和美敦力新胰岛素泵CGM产品批准进一步延迟,糖尿病业务再次受到严重打击,并立即反映在市场上。警告信称,美敦力的股价在几天内下跌了11%以上99.53美元。
2021年度召回事件也多次涉及中国产品。
20212012年12月,国家食品药品监督管理局宣布,由于制造错误,美敦力 Covidien 部门已经启动Puritan Bennet 980 系列呼吸机一级召回。
202111月18日,国家食品药品监督管理局发布了多起美敦力召回事件,其中胰岛素注射泵Insulin Pump和对膜支架系统Endurant II Stent Graft System一级召回。
救命神器一级召回,占中国的50%
随着2022年新年的到来,美敦力的召回事件并未结束。
仅一个月前,美敦力就涉及四起案件I等级召回包括:
Covidien的PuritanBennett 980 系列呼吸机Synergy Cranial 、Stealth Station S7 Cranial 软件和HawkOne定向切除系统
然而,就在大家对召回事件并不陌生的时候,这次一级召回其实涉及到中国50%的产品。
2022年3月,NMPA美敦力决定对公告作出决定(ECMO)离心泵血液控制监测系统Extracorporeal Blood Pumping Console产品一级召回。
文件显示,故障可能导致仪器关闭,包括界面变黑、设备冒烟和使用过程中燃烧的气味。
业内人士解读,对ECMO对于机器,黑屏或血泵停止意味着机器不能正常模拟人体血液循环。虽然概率不高,但结果极其严重。
召回涉及中国生产(进口)263台,目前国内生产(进口)263台。ECMO数量只有500台左右,美敦力召回涉及的设备几乎占了一半。
ECMO除了暂时替代患者的心肺功能,减轻患者的心肺负担外,如呼吸衰竭、心脏骤停等,也被称为救命神器。
中国ECMO产品部署不足,但ECMO它也是当前疫情防控中急需的重点医疗设备。可以说,召回对我国医疗体系影响很大。
03
业务增速放缓
此前,美敦力发布了2021财年全球财报数据(FY21周期为2020年4月25日至2021年4月30日)。
数据显示,2021年美敦力财年公布的收入为301.17报告收入增长4%,有机增长率为2%。
其中,四大板块的具体财务表现如下:
心血管业务实现收入107.72亿美元,同比增比2.9%手术和重症业务实现收入87.37亿美元,增长4.6%,神经科学业务实现81.95亿美元,同比增长6.1%,糖尿病业务实现24.13亿美元,同比增长1.9%。
*2021年美敦力财年区间为2020年4月28日至2021年4月28日。
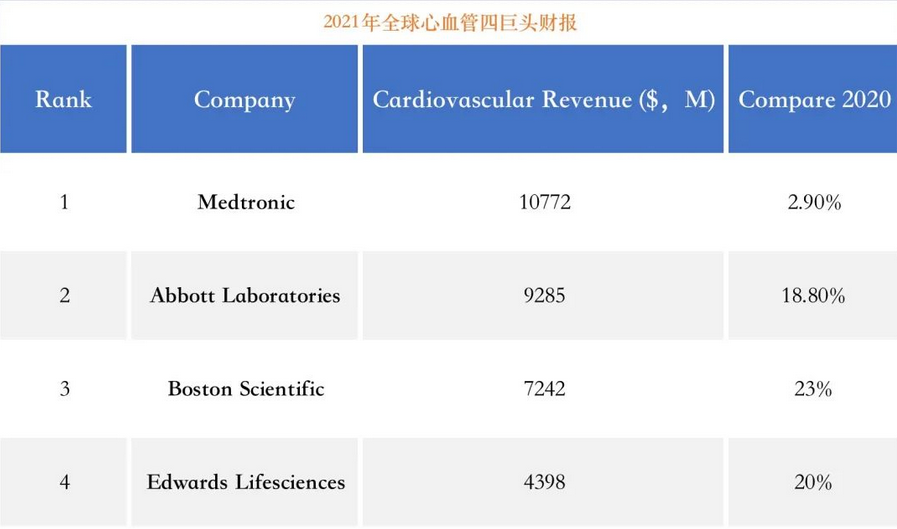
结合其他公司最近的财务报告,全球四大心血管巨头保持不变:美敦力第一,雅培第二,波士顿科学第三,爱德华生命科学第四。
虽然美敦力在心血管领域仍占据第一,但增速明显减弱,在四家公司中增速最低。
2021财年也是Geoff Martha作为美敦力全球CEO2021财年最后一季度,美敦力调整了心脏节律与心力衰竭、结构性心脏病、主动脉、冠状动脉和外周血管等心血管业务结构,寻求改变。
心血管业务是美敦力最早、开展业务时间最长的业务,也是收入最高的业务。2020财年,该业务板块收入下降9%,2021财年业绩下
截图来自美敦力财报
受胰岛素泵召回事件影响,2022财年前三个季度(截至2022年1月28日),美敦力糖尿病业务收入17.41亿美元,同比下降1.4%,是美敦力唯一下跌的业务板块。
此次Harmony经导管肺动脉瓣(TPV)导管系统的召回给美敦力的心血管部门敲响了警钟。然而,作为世界上第一个自膨胀肺动脉瓣,该产品的创新价值仍然值得肯定。
在之前的临床研究中Harmony经导管肺动脉瓣(TPV)它还表现出优异的安全性(无死亡率)和有效性。
在一项前瞻性、非随机、多中心的临床研究中,70名患者被植入Harmony。所有患者都计划在研究开始、植入、出院和植入后一个月、六个月和五年进行随访。
Harmony植入后30天内,主要安全终点为无手术或器械相关死亡,100%的患者实现了这一目标。6个月内无明显再干预、再手术或心内膜炎。同时,在可评估超声心动图的患者中,89.2%达到主要疗效终点。
Harmony获批后,本研究推迟至10年,以提供Harmony长期耐久性、安全性和有效性。
医疗器械直接关系到人体的安全,因此其创新过程和上市尤为困难。未来召回的影响会扩大吗?设备之家将继续关注。