南京圣和药业深入布局丙肝领域!获得达拉他韦首仿,创新药报上市
发布时间: 2022-04-08 19:52:35
20222004年4月6日,药品批准证明文件发布,共批准受理号175个。值得注意的是,南京盛和药业的丙型肝炎病毒口服药物盐酸达拉他韦片获批。此前,只有3种产品规则获得批准,没有国内企业获得批准。南京圣和药业被批准为中国第一种仿制药。此外,据调查,南京圣和药业深入布局丙型肝炎领域,其全基因丙型肝炎创新药物奥磷布韦正处于上市阶段。


截图来源:NMPA官网
韦原研究来自达拉他Bristol-Myers Squibb Co(百时美施贵宝)是第一个抗丙肝病毒的人NS5A抑制剂。盐酸达拉他韦片015年,盐酸达拉他韦片(商品名和2015年在日本、欧洲和美国获批治疗丙型肝炎病毒感染。2017年4月BRISTOL-MYERS SQUIBB (SINGAPORE) PTE. LTD.盐酸达拉他韦片首次在中国获批上市,这也是中国首次上市的丙型肝炎直接抗病毒药物。
丙型病毒性肝炎,简称丙型肝炎、丙型肝炎,是一种丙型肝炎病毒性肝炎(HCV)感染引起的病毒性肝炎主要通过输血、针灸、吸毒等传播。据世界卫生组织统计,全球卫生组织统计,全球卫生组织统计,HCV感染率约3%(估计约3%)1.81亿人),患者群体庞大。未来20年内和未来20年内,患者群体。HCV与感染相关的死亡率将继续上升,对患者的健康和生命造成极大的危害,并已成为一个严重的社会和公共卫生问题。
经查询,截至目前,我国共有三品规盐酸达拉他韦片上市,均来自中国BRISTOL-MYERS
SQUIBB(SINGAPORE) PTE. LTD.进口药品,无国产批准。南京圣和药业获批为国内首仿。
盐酸达拉他韦片药品批文信息
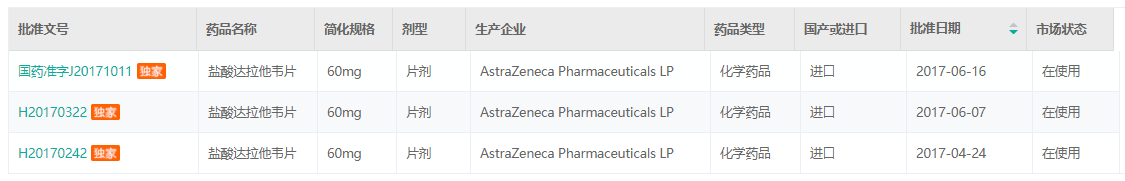
截图来源:药云中国药品批文数据库
根据CDE目前披露信息CDE共有6份盐酸达拉他韦片申请,其中只有3份国产药品上市登记申请,分别来自南京盛和药业和扬子江药业。
盐酸达拉他韦片承担信息
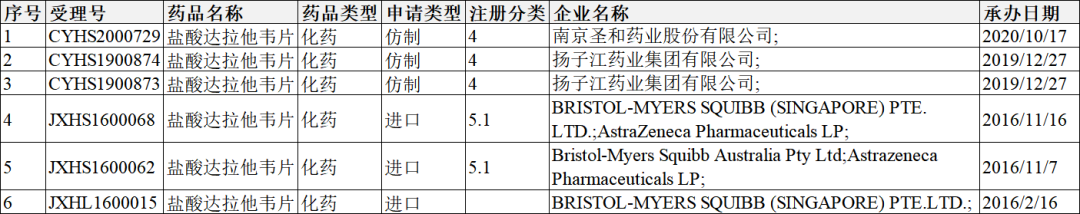
截图来源:CDE官网
根据南京盛和药业官方网站披露的信息,公司深入布局丙型肝炎领域,另一种全基因丙型肝炎创新药物奥磷布韦(alfosbuvir)正处于申报上市阶段。奥磷布韦是南京圣和药业自主研发的中国家奥磷布韦公司HCV NS5B聚合酶抑制剂也是合酶抑制剂也是世界上第二个完成聚合酶抑制剂III期临床研究并提交上市申请HCV NS5B抑制剂。
根据相关临床研究数据,奥磷布韦治疗慢性丙型肝炎成人患者疗效显著,治疗效果优于同类产品,安全性好(本研究期间未发生受试者死亡)。实验证明,奥磷布韦是我国丙型肝炎治疗领域的重大突破,是我国原创丙型肝炎DAA药物为治疗泛基因型慢性丙型肝炎提供了有力的证据,为我国慢性丙型肝炎患者提供了更好的治疗选择。
奥磷布韦的基本信息
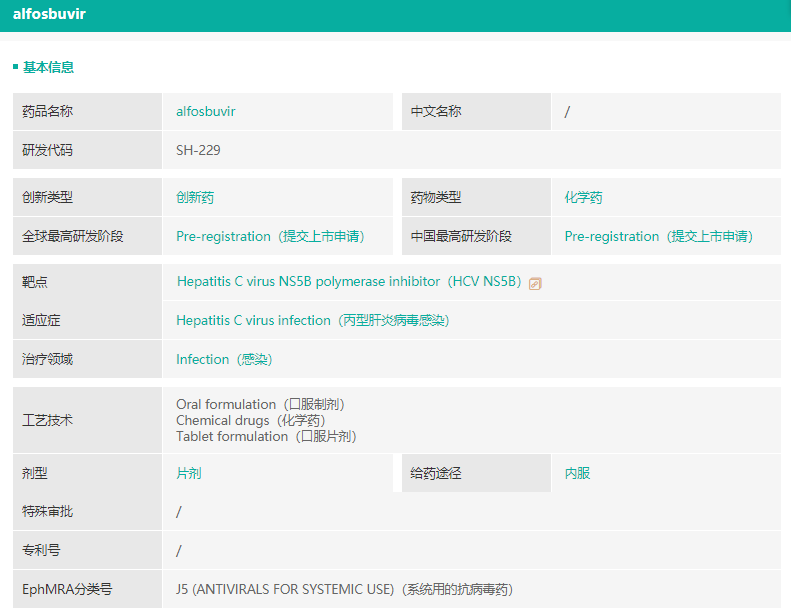
截图来源:药融云全球药物研发数据库
南京圣和药业研发管线

来源:南京圣和药业官网
