Biogen:第二款阿尔茨海默病药物急需申报,能否摆脱Aduhelm的阴影?
发布时间: 2022-05-13 10:39:58
引言
本周,渤健(Biogen)和合伙人卫材(Eisai)他们宣布,他们已经完成了为期8个月的阿尔茨海默病(AD)新药lecanemab提交滚动申报。尽管如此。lecanemab的大型III临床研究的试验结果预计要到明年秋天才能公布,Biogen和卫材对这种药还是寄予厚望的,卫材说甚至可能在这个财政年度FDA(美国食品药品管理局)提交lecanemab申请完全批准。
根据药融云数据库,lecanemab是Biogen和卫材在Aduhelm然后推出第二个目标Aβ阿尔茨海默病药物,淀粉样蛋白。
lecanemab基本信息
截图来源:药融云全球药物研发数据库
Aduhelm阴影下的Biogen
一年前,Aduhelm这种阿尔茨海默病药物通过非常规加速批准获得批准Biogen带来了非常大的负面影响,使Aduhelm成为了FDA历史上最具争议的上市药品之一。
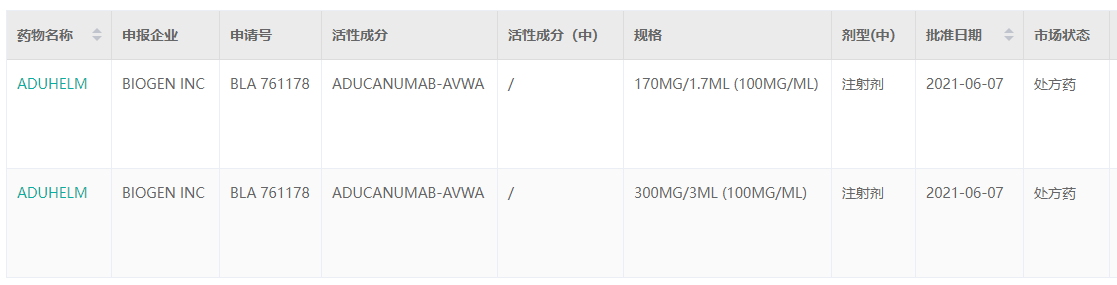
Aduhelm药品批准信息
截图来源:药融云美国FDA批准药品数据库
Biogen曾预测Aduhelm在获得FDA经过快速批准,销售额将达到数十亿美元,但结果是,这种曾经被称为改变阿尔茨海默病治疗方法的药物在上市一年后只被少数患者使用。美国医疗保险和医疗补贴服务中心(CMS)也不愿意为Aduhelm提供医疗保险覆盖。Biogen曾经试图为Aduhelm辩护和采取措施将价格降至28000美元/年,但到今年4月,持续恶化的局面让Biogen要下定决心放弃Aduhelm。4月22日,Biogen宣布撤回Aduhelm申请在欧洲上市。然后,领导Aduhelm项目的Biogen公司CEO Michel Vounatsos离职,Aduhelm营销团队也被解散。
在Aduhelm上市后,Biogen由于负面新闻,股价大幅下跌,至少受到了影响FDA,HHS(Health and Human Services),SEC(美国证券交易委员会),FTC(联邦贸易委员会)和国会派出的调查委员会进行了六次调查,并对其进行了调查FDA密切联系和Aduhelm如何获得批准。Biogen也曾陷入被收购的传闻。在这种情况下,Biogen急于寻求新的出口也就不足为奇了。但阿尔茨海默病药物也是用来清除淀粉样蛋白的,lecanemab真的能给Biogen和卫材带来好运?
lecanemab的前景
lecanemab提交的申请是基于早期诊断为淀粉样病变的856人AD病人的概念验证IIb期数据;以及生物标志物和安全数据,包括180名受试者的开放标签扩展研究;还有来自1,795的确认受试者Clarity AD III盲法安全数据。FDA告知Biogen和卫材,Clarity AD可以作为验证lecanemab这种宽松的条件类似于临床效益的验证性研究FDA曾给予Aduhelm的待遇。
同样令人担忧的还有lecanemab面临的和Aduhelm同样的ARIA-E(淀粉样蛋白相关影像学与水肿/积液有关)以及其他安全问题,以及一个更深层次的问题:去除淀粉样蛋白与阿尔茨海默病患者的临床益处之间是否存在不可避免的联系?我们知道,它存在于大脑中β淀粉样蛋白(A?) 是阿尔茨海默病的生物标志物之一,但其真正的致病机制尚不清楚,靶向治疗是否根据其作用机制产生疗效尚未确定。事实上,随着对衰老和阿尔茨海默病机制研究的深入,现有的AD药物研发管道的靶点不再局限于β淀粉样蛋白(Aβ)和tau根据2021年的说法,这两个生物标志物AD药物发现基金会(ADDF)《阿尔茨海默病2021年临床试验报告》,统计期间临床开发阶段的118款,旨在改变AD77%的治疗是针对疾病进程的药物Aβ和tau其他创新目标。
Aβ目标研发现状
根据药融云数据库,截至目前,Aβ目标创新药物研发共167条,只有两项获批上市。Biogen卫材的Aduhelm中国海洋大学GV-971。此外,提交上升申请的除外Biogen卫材的lecanemab,还有一款礼来donanemab。
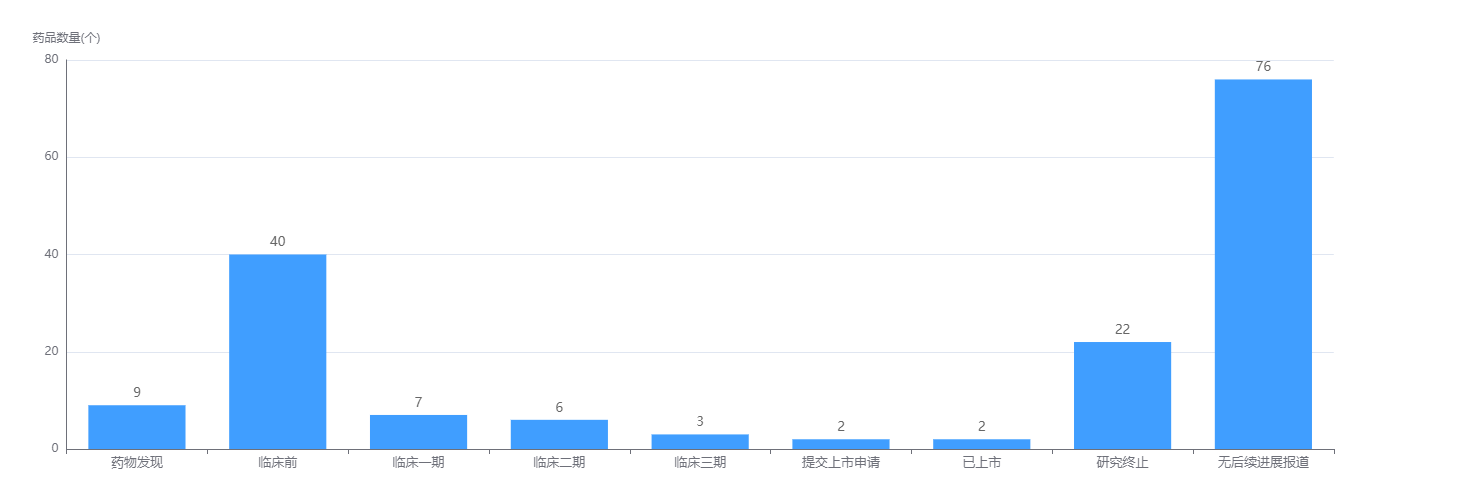
Aβ目标药物研发阶段
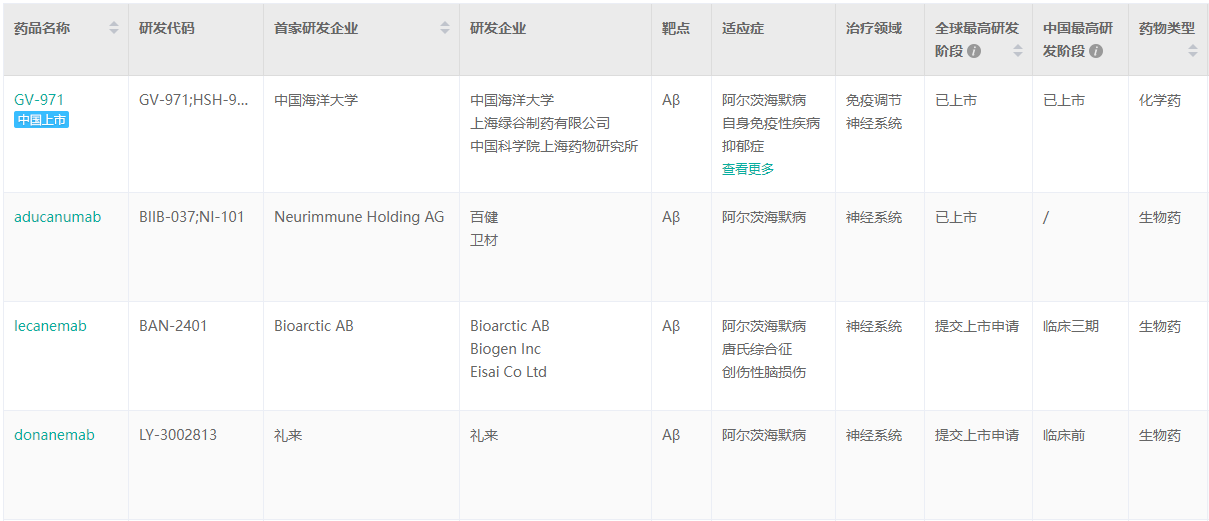
Aβ提交上市申请的目标上市药物
截图来源:药融云全球药物研发数据库
小结
不管Biogen的lecanemab最终的结果是什么?阿尔茨海默病药物的临床缺乏也是不争的事实。Aduhelm阿尔茨海默病是近20年来首次获准上市,其失败可能成为未来治疗阿尔茨海默病药物成功的敲门砖。
参考来源:
[1] FDA官网
[2]https://www.pharnexcloud.com/?zmt-xlyy
[3]Biogen
[4]
[5] Alzheimer's Drug Discovery Foundation | alzdiscovery.org