十多年来,第一种治疗帕金森病的新药!「沙芬酰胺」在中国申报上市
47月7日,中国国家食品药品监督管理局药品评价中心(CDE)官方网站公布了一款名为沙芬酰胺片的官方网站5.1新药在中国提交上市申请并受理。公开资料显示,沙芬酰胺。(safinamide)2017年获得美国帕金森病治疗新药FDA该批准已成为美国第一个用于治疗帕金森病的新化学实体。
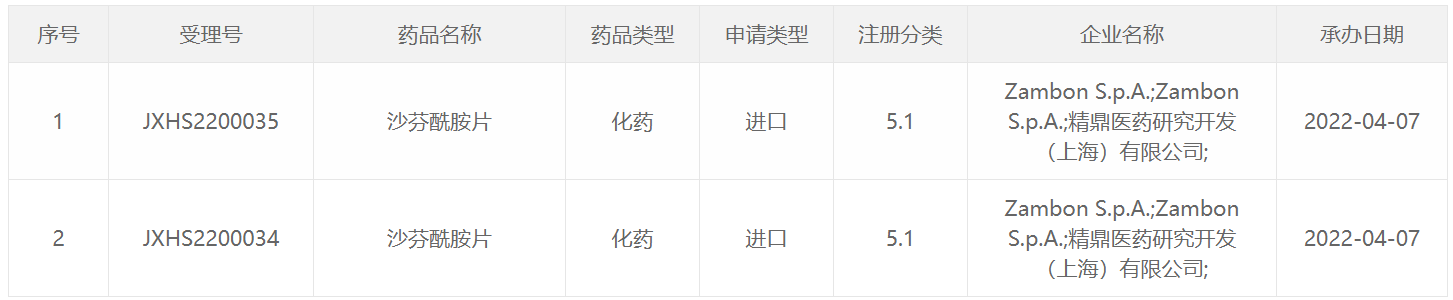
截图来源:CDE官网
帕金森病是一种常见的中老年神经系统退行性疾病。左旋多巴是改善帕金森病患者临床症状的标准治疗方法。然而,随着疾病的发展和长期使用,大多数患者对药物不敏感,症状波动。这种波动分为两个阶段——在开放期间,患者的运动能力正常;在关闭期间,患者的运动能力会显著下降,甚至很难行走。这些患者需要额外的药物来处理和管理服用左旋多巴引起的运动能力波动。
公开数据显示,沙芬酰胺是一种具有独特功能的新型化学实体,包括选择性和可逆性单胺氧化酶B(MAO-B)抑制和阻断电压依赖性钠通道,从而调节谷氨酸的异常释放。MAO-B它可以降解多巴胺,多巴胺可以在大脑区域传递信号,这对流畅的自主运动非常重要。因此,沙芬酰胺有望避免多巴胺被多巴胺覆盖MAO-B降解可以缓解帕金森病患者在关闭期间的运动能力下降。临床试验证明,沙芬酰胺可以在短时间内控制帕金森病患者的运动症状和并发症,并可以持续两年。
根据公开信息,沙芬酰胺由沙芬酰胺组成Newron Pharmaceuticals研发,由Zambon公司、Meiji Seika、卫材(Eisai)、Supernus Pharmaceuticals公司负责商业化。2017年3月,FDA宣布批准沙芬酰胺片(商品名称)Xadago)帕金森病患者目前正在服用左旋多巴/卡比多巴并出现关闭期。
根据FDA沙芬酰胺的疗效在645名帕金森病患者和549名帕金森病患者参加的两项临床试验中得到证实。与服用安慰剂的患者相比,服用沙芬酰胺的患者显著延长了开放期,缩短了关闭期。此外,在开放期,患者的运动功能指标得分优于治疗前,没有无法控制的运动。
根据中国药物临床试验登记和信息宣传平台的信息,沙芬酰胺作为特发性帕金森病辅助治疗的第三期临床研究已经完成。本研究旨在评估沙芬酰胺作为辅助治疗的中国特发性帕金森病患者的疗效,用于接受稳定剂量的左旋多巴治疗和运动波动。该研究包括中国33家临床试验机构的307名受试者,主要研究者是四川大学华西医院商慧芳教授。
沙芬酰胺片在中国提交上市申请,意味着即将来到中国,从而造福更多帕金森病患者!
参考资料:
[1]中国国家食品药品监督管理局药品评审中心(CDE)官网.Retrieved Apr 7,2022.From https://www.cde.org.cn/main/xxgk/listpage/2f78f372d351c6851af7431c7710a731
[2]FDA approves drug to treat Parkinson’s disease.Retrieved March 21,2017. From https://www.fda.gov/news-events/press-announcements/fda-approves-drug-treat-parkinsons-disease
[3]FDA APPROVES XADAGO? (SAFINAMIDE) FOR PARKINSON’S DISEASE (PD) PATIENTS.Retrieved Mar 21,2017.From https://www.newron.com/news-and-media/regulatory-news/fda-approves-xadagor-safinamide-parkinsons-disease-pd-patients
