深度综述:RNA治疗的进展和展望
随着mRNA基于新冠肺炎疫苗的成功开发和多种RNA新药获批,RNA已经跃居药物研究前沿。mRNA不同类型的蛋白质产生抗原或治疗性蛋白质RNA它还具有多种功能,在细胞和组织中起着重要的调节作用。RNA作为一种新一种新疗法的潜力RNA既可以作为药物,也可以作为靶点。
最近,发表了一篇文章Journal of Medicinal Chemistry上面的综述文章是基于对的CAS内容合集(CAS Content Collection)不同类型的分析和评估RNA在医学应用中的优势和挑战。同时也是对的RNA治疗和疫苗开发管道RNA总结了化学修饰和交付机制。在本文中,姚明康德内容团队将与读者分享精彩内容。点击文章末尾阅读原文/Read more,即可访问原始论文页面。

RNA类型及其在医学中的应用
RNA它是一种多功能生物大分子,可以广义定义为编码RNA和非编码RNA(ncRNA)。ncRNA包括多种类型tRNA、lncRNA、miRNA、小干扰RNA(siRNA)、saRNA、circRNA、和外泌体RNA各种类型RNA类型在医学上有不同的应用。mRNA可作为治疗、诊断生物标志物或治疗靶标。mRNA有缺陷或缺失的蛋白可以通过翻译产生治疗性蛋白来代替。mRNA它也可以用作反义寡核苷酸(ASO)、siRNA、miRNA、适配和抑制tRNA治疗靶点。
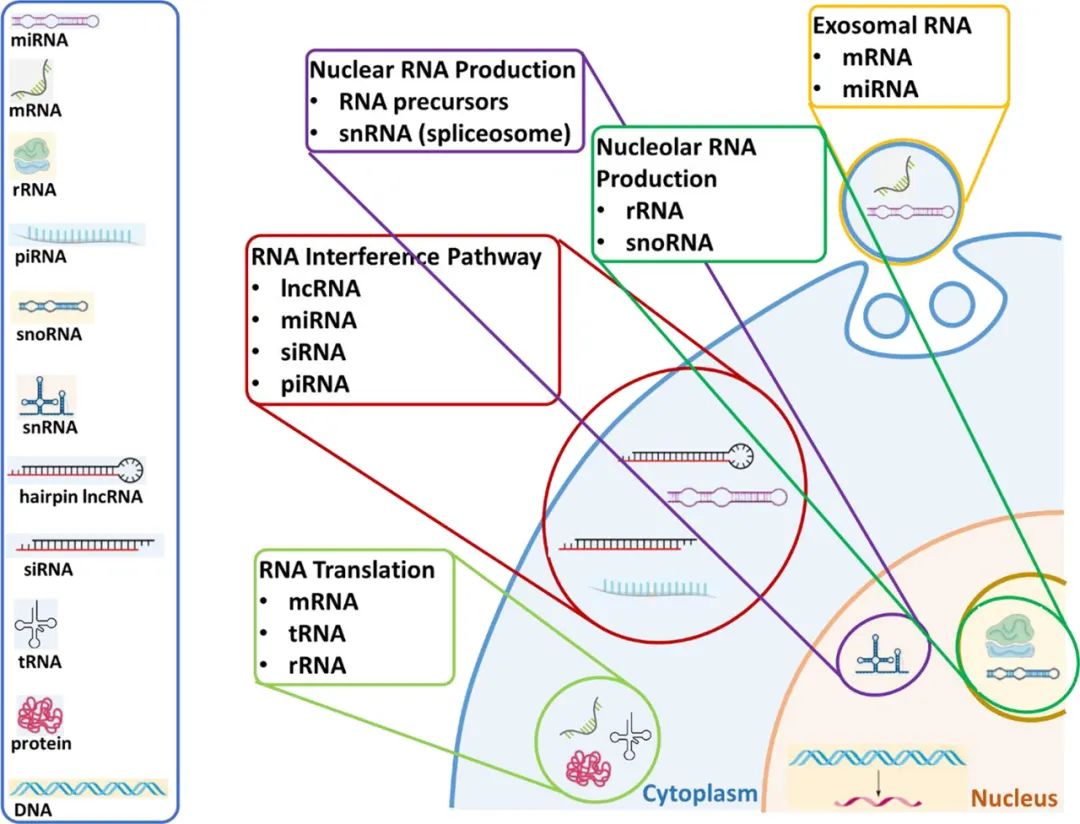
▲不同类型的多种RNA(图片来源:参考资料[1],点击可见大图)
siRNA通过与mRNA编码区域的特定序列组合导致mRNA降解。这种靶向特异性增加了它作为潜在药物的可能性。ASO互补识别DNA或RNA它能促进正常的顺序mRNA剪接,防止表达功能失调的蛋白质,或靶向降解RNA。此外,适配体是构成特定三维结构的寡核苷酸序列。适配体可以结合广泛的目标,包括蛋白质、细胞、微生物、化合物和其他核酸。它与蛋白质的结合可以抑制蛋白质之间的相互作用,从而产生治疗效果。
RNA治疗的优点和挑战
RNA治疗有几个重要优势,包括对目标的高度特异性,通过替换RNA该序列可以在药代动力学和药效学中模块化、可预测性以及相对安全性(其中大多数不会改变基因组)。然而,尽管如此,这种面临着一些挑战RNA即插即用的模块化设计理念可用于治疗药物设计,但仍需通过测试确定其疗效和安全性;因为RNA它很容易降解,所以如何实现细胞传递面临重大挑战。
研发管线中RNA类型及其靶向疾病
回顾过去RNA许多关键临床发现促进了研究RNA不断创新和发展治疗。目前主要的RNA疗法包括mRNA,小干扰RNA等。
然后是1960年对核酸的早期研究mRNA从那以后,大约60年后,人类终于通过了对抗mRNA将其应用于临床-开发新冠肺炎mRNA疫苗。现在有两个新冠肺炎mRNA美国获得疫苗FDA上市批准。与传统疫苗相比,mRNA疫苗合成和生产工艺相对方便,具有较强的免疫原性,不需要传统疫苗必需的辅助剂。
就siRNA来说,2006年Andrew Fire博士和Craig Mello博士发现RNA干扰机制获得诺贝尔医学或生理学奖。2010年人类关键临床试验表明,siRNA它可以靶向特定的人类基因,随后的临床前研究和开发可以促进第一种siRNA疗法——Onpattro(patisiran)2018年获批批准,用于治疗由遗传性转甲状腺素蛋白淀粉样变性(hATTR)引起周围神经系统疾病的成年患者。目前已获得批准siRNA疗法还有Givlaari(givosiran)、Oxlumo(lumasiran)和Leqvio(inclisiran)。
反义寡核苷酸的使用(ASO)1978年就提出了作为疗法的概念,20年后第一次ASO药物Vitravene(fomivirsen)获得美国FDA批准。现在,已经有很多款了ASO药物获得美国FDA批准。
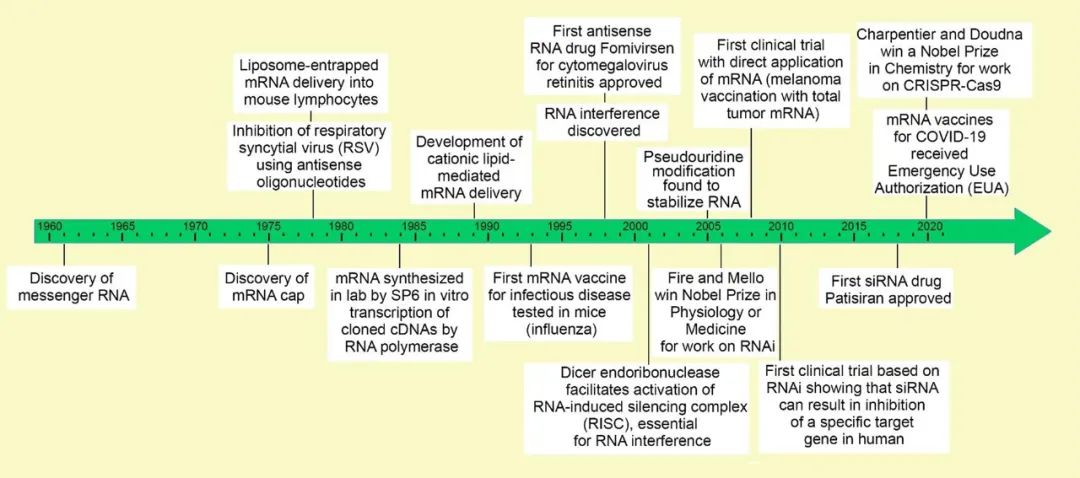
▲RNA关键研究和开发里程碑(图片来源:参考资料[1],点击可见大图片)
RNA该技术为开发罕见或难治性疾病的新药提供了一种创新的方法。目前,正在研究一些模型RNA治疗处于不同的临床前和发展阶段,包括癌症、肝肾疾病、心脏病、代谢性疾病、血液疾病、呼吸系统疾病和自身免疫性疾病。
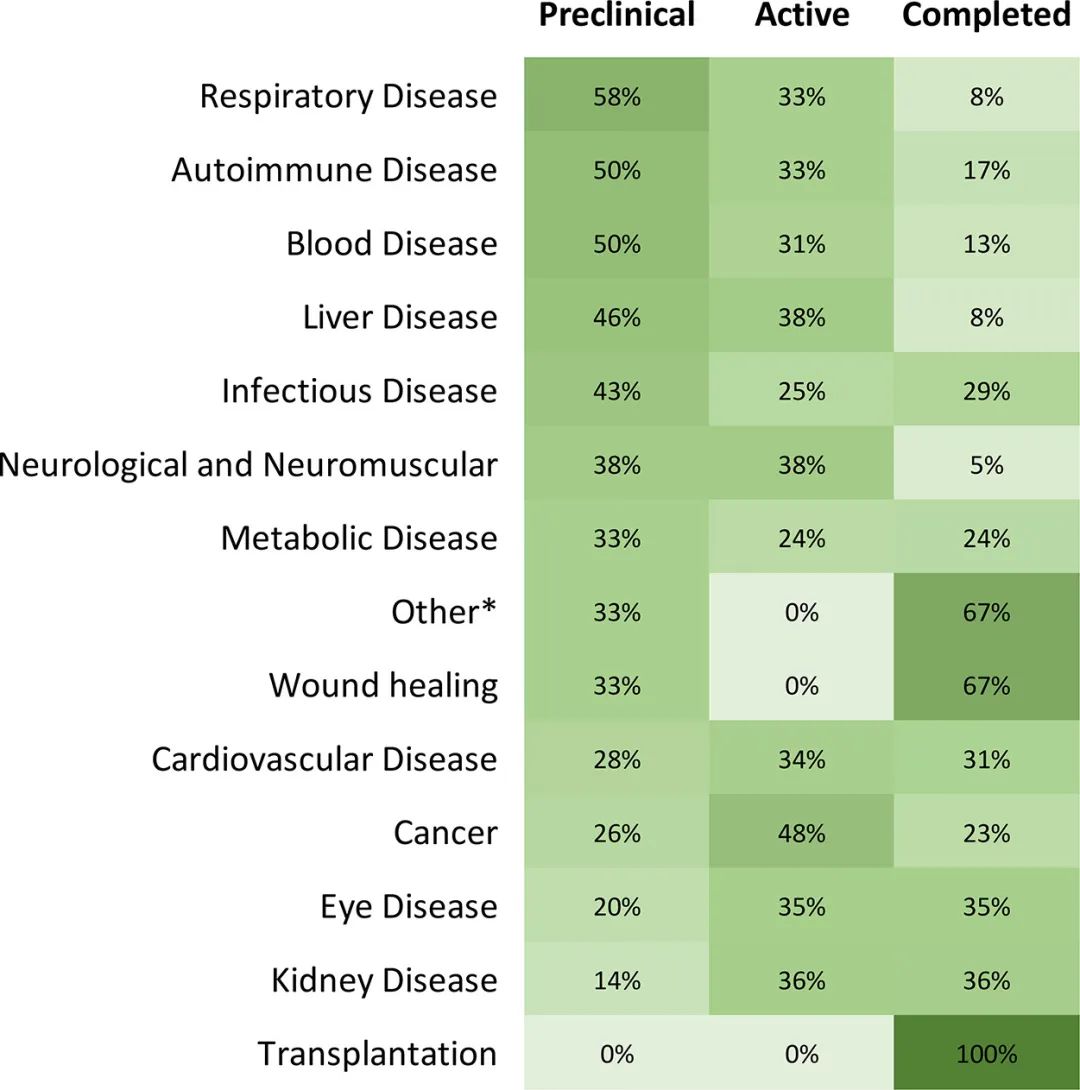
▲在研究管道开发阶段分布治疗不同疾病(图片来源:参考资料[1])
与其它生物分子相比,RNA分子不稳定。RNA分子进入人体后,细胞中的蛋白质表达水平有限,这通常会导致人体内的免疫反应。这些问题可以解决RNA各种分子优化(包括化学修饰等)缓解。
可以通过化学修饰来改善RNA稳定性和靶向特异性
化学修改可以保护治疗RNA不受核酸外切酶、核酸内切酶和细胞环境的影响,增强药物活性。骨骼的选择决定了骨骼的选择ASO它是否阻断了细胞过程,如翻译、转录或剪接,或靶向RNA消化核酸酶siRNA可以通过减少核糖的修改来修改siRNA热稳定性降低了脱靶效应,从而增强了与靶标的特异性结合。1-甲基假尿嘧啶核苷可改善治疗性mRNA稳定性和翻译。
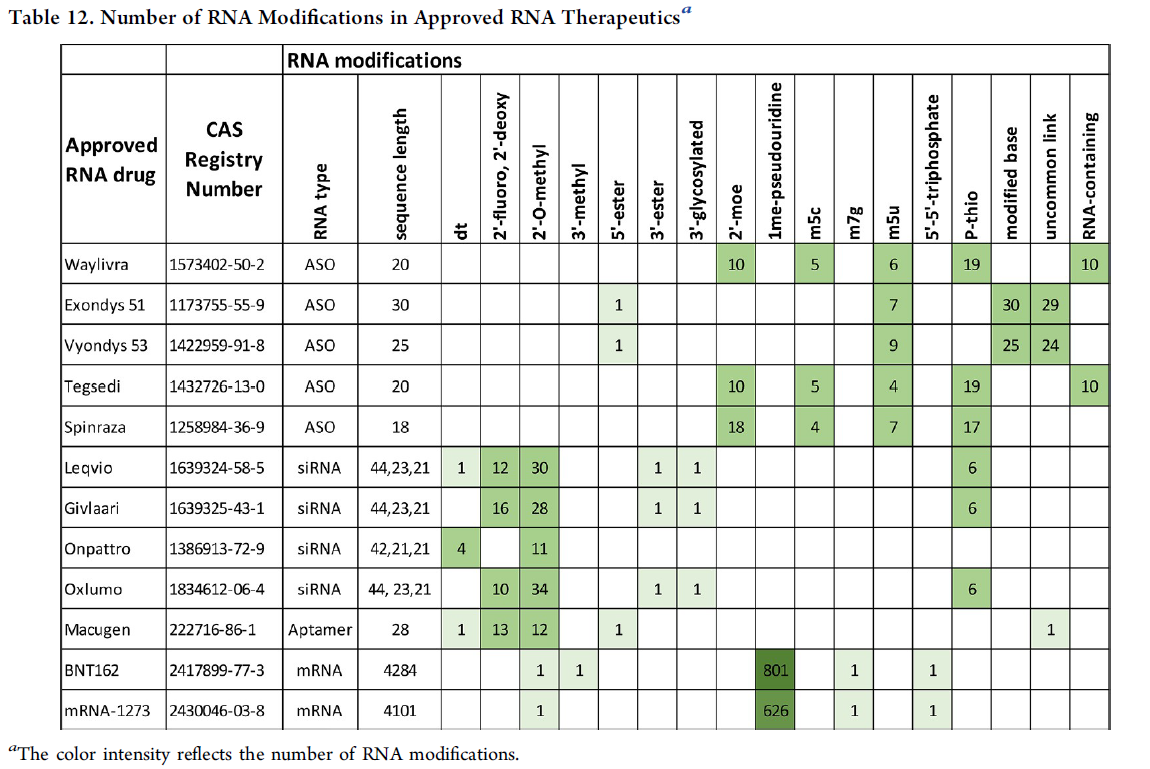
▲获批RNA化学修饰疗法(图片来源:参考资料[1],点击可见大图)
RNA递送系统
带负电荷的亲水性RNA治疗药物不能通过细胞膜,因此它们需要交付载体和/或化学修改才能达到其目标。尽管生物障碍,如免疫原性和核酸酶,通常可以通过匹配RNA化学修饰会解决,但会解决RNA包裹到纳米载体可以保护RNA,它也可以传递给细胞。纳米材料具有生物降解性、生物相容性和低毒性,也可以用作RNA载体。包括脂质、壳聚糖、环糊精、聚乙烯亚胺(PEI)、聚乳酸-乙醇酸、树状大分子、磁性纳米颗粒、碳纳米管、金纳米颗粒、二氧化硅纳米颗粒等。
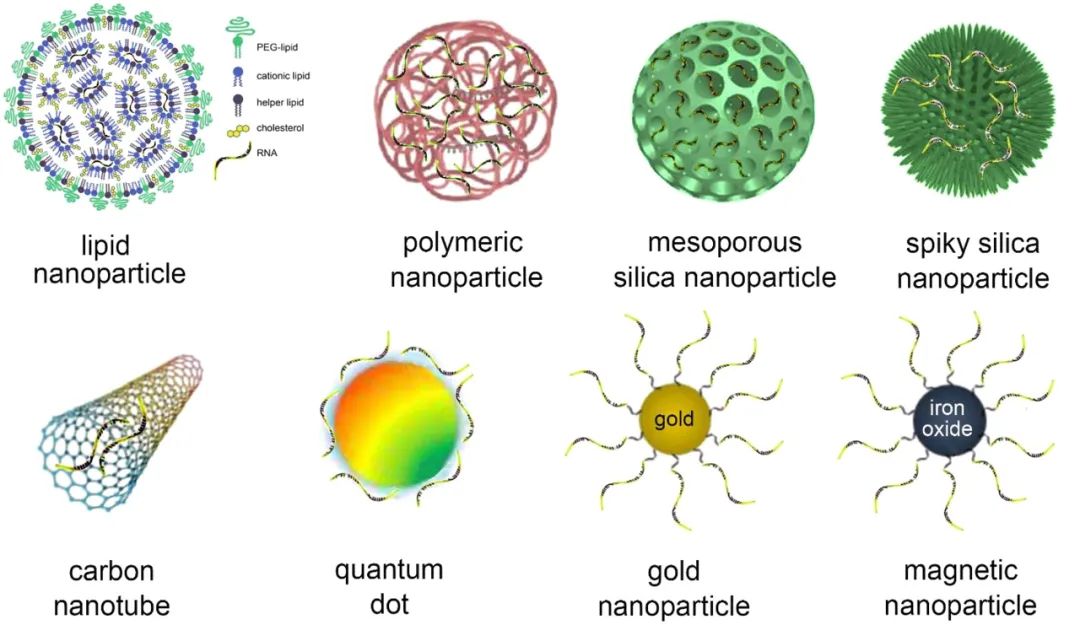
▲递送RNA载体类型(图片来源:参考资料[1])
脂质纳米颗粒是目前应用最广泛的核酸药物和疫苗的非病毒传递系统之一。其优点包括易于生产、生物降解、保护核酸免受核酸酶降解和肾清除、促进细胞摄入和内逃逸。最近,脂质纳米颗粒被用作mRNA新冠肺炎疫苗的重要组成部分引起了全球的关注mRNA在细胞中起着关键作用。
聚合物是仅次于脂质的第二大核酸输送载体。阳离子聚合物与阴离子核酸形成稳定的复合物,为高效核酸输送提供了一个通用、可扩展和易于调节的平台,同时最大限度地降低免疫反应和细胞毒性。线性阳离子聚合物也是研究最广泛的载体之一。此外,多肽在结构和功能上具有多样性和生物相容性,可用于靶向细胞。
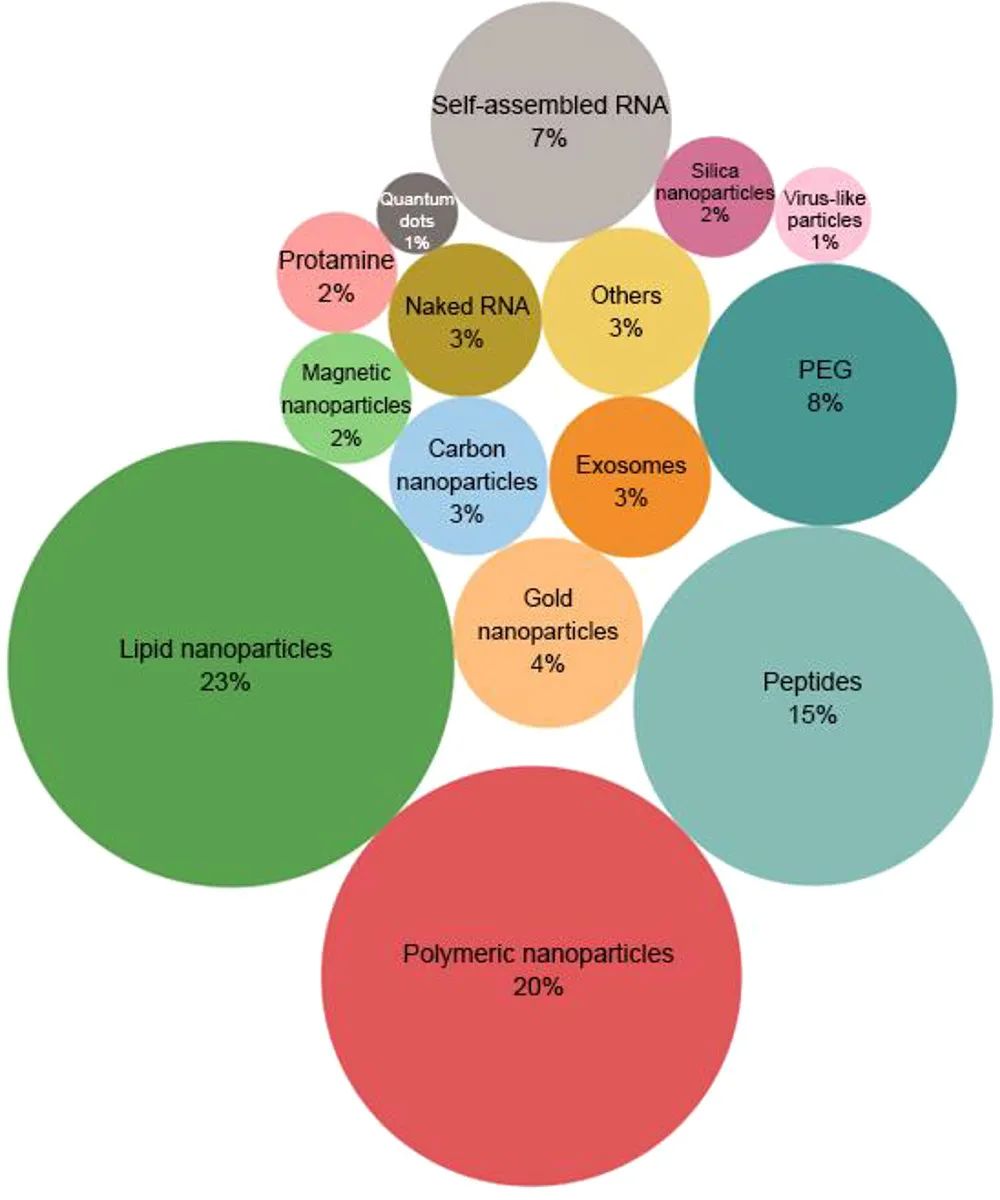
▲不同RNA递送载体在CAS内容集中出现比例(图片来源:参考资料[1],点击可见大图)
结语
综上所述,RNA药物已被批准用于治疗心血管于治疗心血管、代谢、肝脏、感染、神经、神经肌肉、肾脏和眼部疾病。RNA克服目标的载体RNA药品交付面临的挑战具有重要意义。作者说,随着我们的发展,RNA进一步了解多种类型和功能,产生更高的稳定性和药物活性RNA能力逐渐提高,基于纳米技术的载体可以使这些载体RNA靶向递送到细胞,具有多种特异性的靶向递送RNA治疗选择呈爆炸式增长,具有彻底改变人类疾病治疗的潜力。
参考资料
[1] Sasso JM et al.,(2022),The Progress and Promise of RNA Medicine─An Arsenal of Targeted Treatments. J Med Chem,https://doi.org/10.1021/acs.jmedchem.2c00024
