治疗乳腺癌 第一、三共/阿斯利康Enhertu再获FDA突破性疗法
4月27日,阿斯利康和第一三联合宣布HER2ADC药物Enhertu已获得FDA突破性疗法(BTD),在辅助治疗后6个月内复发或进展至少一次全身治疗HER2低表达(IHC1 orIHC2 /ISH-阴性)不能切除或转移性乳腺癌患者。
这是Enhertu第三种是乳腺癌BTD。Enhertu此前曾于2021年和2017年获得二线HER2阳性转移性乳腺癌HER2阳性转移性乳腺癌的突破性治疗。
DESTINY-Breast04随机、开放标签、全球多中心注册III期临床、评价Enhertu(5.4mg/kg)与医生选择的化疗(卡培他滨、艾日布林、吉西他滨、紫杉醇或白蛋白紫杉醇)在一起HR阳性(n=480)或HR阴性(n=60)的HER2低表达不可切除和/或转移性乳腺癌患者的疗效和安全性,这些患者以前接受过一两种化疗方案。患者按2:1随机分组接受Enhertu或化疗。主要终点是BICR评估的HR阳性患者的PFS,关键次要终点包括BICR所有被评估的病人PFS、HR阳性患者及所有患者OS。
结果显示,DESTINY-Breast04达到其主要终点,并达到其主要终点SOC相比,Enhertu在过去的经治中HR阳性HER2低表达转移性乳腺癌患者表现更好PFS。同时,试验也达到了所有关键的次要终点,无论是否HR表达状态如何,都显著患者PFS和OS。安全性与以往临床试验一致,未发现新的安全信号。
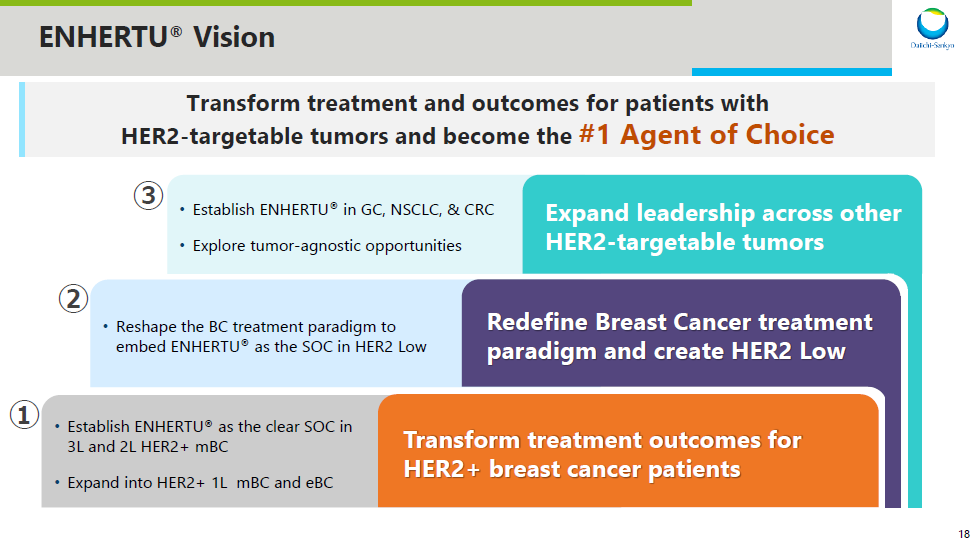
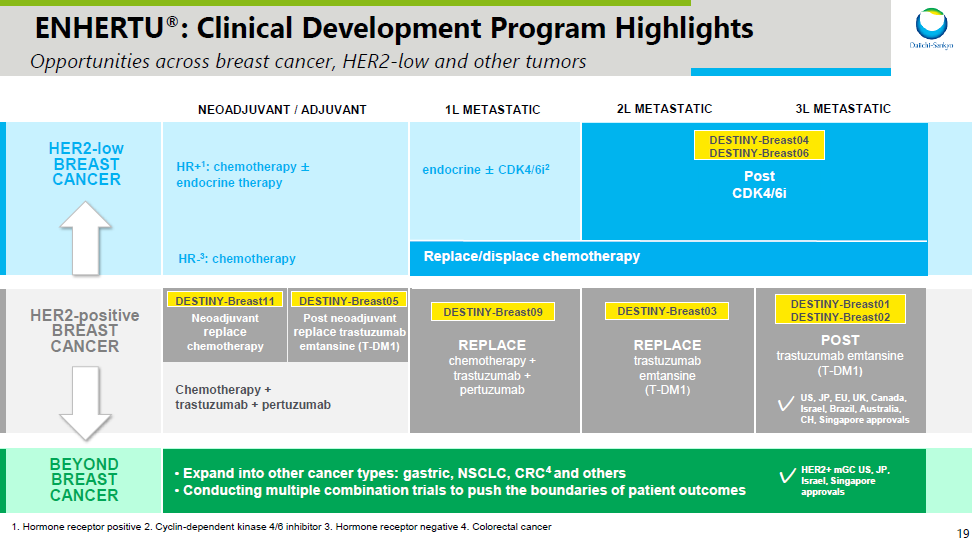
DESTINY-Breast04研究的突破有望推动阿斯利康和第一、三共领先利用ADC药物涵盖了乳腺癌治疗的整个领域,包括在不同的领域HER2表达状态和差异HR探索表达状态。与此同时,除了广泛的覆盖之外,第一和第三共和国阿斯利康还在推动这些疗法向更前沿发展(详见下图)。乳腺癌之后,还将探索Enhertu在胃癌(GC)、非小细胞肺癌(NSCLC)、结直肠癌(CRC)中的疗效。
Enhertu(HER2)乳腺癌开发计划