奥赛康厚积薄发40亿品种!
近日,奥赛康又有一类新药获批临床,ASKC202片将用于晚期实体瘤治疗的临床试验。近年来,奥赛康加强了研发,初步完成了从第一仿制、仿制结合到创新药物、高端第一仿制药的产品转型升级,公司第一类新药ASK预计今年将批准120067片。此外,临床上还批准了4种1类新药,其中3种是抗肿瘤药物,未来将共同为公司抢占1000亿市场。此外,备受业界关注的第七批国采近日正式正式宣布,奥赛康将有4款产品参与新一轮激战。
四颗抗肿瘤新星聚焦千亿市场,第一类新药备受关注
近年来,随着国内制药企业研发能力的不断提高,国内创新药物如雨后春笋般涌现。同时,抗肿瘤领域一直是一个备受关注的重大疾病领域,国内抗肿瘤创新药物门领域。
另一方面,随着国内新药的上市,为患者提供了更多质优价廉的用药选择,进一步推动了国内抗肿瘤药物市场规模的上升。根据米内网的数据,2013年,中国城市公立医院、县级公立医院、城市社区中心和乡镇卫生院(以下简称中国公立医疗机构)终端抗肿瘤和免疫调节剂的市场规模仅为724亿元,2020年上升至1600多亿元。
面对潜力巨大的药品市场,奥赛康也抓住了创新药物的布局。截至目前,奥赛康已有1种新药报生产并正在审查中,2种化学品1种新药获批临床实践,2种生物药物1种新药获批临床实践,5种1种新药中有4种集中在抗肿瘤领域。此外,一种新药涉及近年来热门的眼科用药领域。
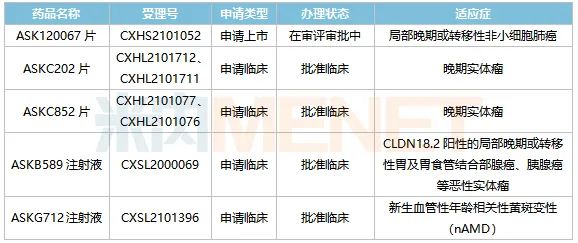
ASK120067片是靶向作用T790M的第三代EGFR抑制剂,用于治疗非小细胞肺癌,奥赛康于2017年获得临床批准,随后以突出为基础I/II期临床研究成果,公司于2019年取得了期临床研究成果CDE许可,完成II2021年11月,奥赛康提交上市申请,预计今年最快将迎来好消息。
表2:中国上市的第三代EGFR抑制剂的销售
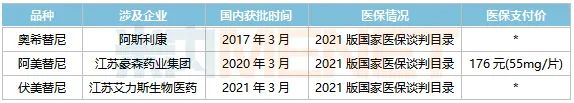
来源:米内网中国医保目录大全数据库
目前国内市场上有三个第三代EGFR抑制剂,阿斯利康的奥希替尼最早于2017年获批进口,随后于2018年成功进入国家医疗保险目录。根据米内网的数据,2020年中国公立医疗机构终端和中国城市实体药店终端的总销售额已超过45亿元。第一个国内第三代EGFR抑制剂阿美替尼于2020年获批,随后谈判成功进入国家医保目录,医保支付价格为176元(55元mg/片);第二款国产第三代;EGFR抑制剂花落艾力斯,伏美替尼成功进入2021版国家医保谈判目录。
ASK作为奥赛康生产的第一种新药,公司对120067片寄予厚望。2021年3月,奥赛康宣布与上海药明康德合作开发新药,该项目不仅用于治疗Exon未来14突变的非小细胞肺癌也将与非小细胞肺癌相结合ASK联合用药120067片;此外,最新批准的临床用药;ASKC未来也将有202片ASK120067片联合用药……从这个角度看,奥赛康将ASK以120067片为基点,以扩大非小细胞肺癌为目标群体,逐步构建公司抗肿瘤药物产品群。
临床批准ASKC202片是一种强大、高选择性的口服小分子c-MET抑制剂,目前的目标c-MET已成为肿瘤治疗领域的研发热点,国际上批准了两种高选择性的MET抑制剂是默克的特泊替尼和诺华的卡马替尼。卡马替尼于2020年5月获得FDA截至2021年,全球累计销售额已达销售额已达1.25亿美元,潜力不容小觑。国产新药赛沃替尼片于2021年获批上市,国内市场仍有待开发。
奥赛康还有一种抗肿瘤化药物,一种新药已获批临床实践,ASKC852片是公司与药明康德联合开发的小分子免疫调节药物。临床前研究表明,新药单药能反映抑瘤作用和抑瘤作用PD-1/L抗体联用显示出显著的协同抗肿瘤作用,还能有效抑制癌细胞的转移。
在抗肿瘤药物领域,奥赛康的第一种生物药物是一种新药ASKB589注射液主要通过589注射液ADCC和CDC杀死肿瘤细胞,计划用于胃和胃食管结合部腺癌、胰腺癌等适应症,目前,I、II临床期正在进行中。
公司第二类生物药一类新药是ASKG712注射液是一种可同时靶向的新药VEGF与ANG2.双特异性抗体能有效改善血管稳定性,减轻视网膜炎症,同时控制新生血管的形成。临床结果表明,ASKG712注射液安全性好,对VEGF和ANG2具有较强的组合活性,有望在临床上达到较好的疗效,减少玻璃体注射的给药次数。
近年来,奥赛康继续加大研发投入,2018年-2020年研发投入分别为2020年.9亿元、3.93亿元、4.营业收入分别占708亿元.38%、8.69%、10.79%,2021年前三季度,公司研发投入同比也有45%.74%的增长。目前,除了抗肿瘤和眼科用药外,奥赛康布局的一类新药也发展迅速。
据悉,ASK0912注射液是奥赛康与中国医学科学院医学生物技术研究所联合开发的创新药物。该新药对临床耐药性严重的革兰氏阴性菌具有广谱活性。许多内外药效研究表明,抗菌活性强于多粘菌素B和E,而且毒性降低,这种新药有望在今年申请临床实践。
仿制药全面升级,四大产品冲击第一仿制药
2021年,奥赛康批准上市的仿制药中,有7种按新分类报告生产,其中2种获得国内独家 国内第一仿制药,2种获得国内第二仿制药。此外,4种报告生产和审查的仿制药有望影响中国的第一种仿制药。
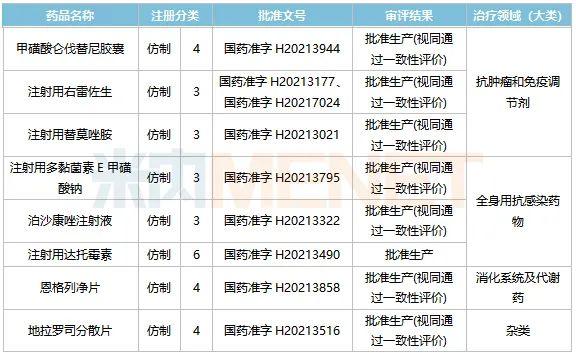
近年来,奥赛康猛攻抗肿瘤领域。除了布局一种新药外,高端仿制药也收获颇丰,其中注射替莫唑胺获得国内第二名。
全身抗真菌药泊沙康唑注射液是默沙东的重量级产品。奥赛康获得了中国第一个仿制品。同时,公司早些时候获得了泊沙康唑肠溶片在中国大陆的独家推广权,可以形成序贯治疗,具有很强的产品组合优势。此外,该公司还获得了多粘菌素注射E据悉,奥赛康药业是唯一一家采用进口原料药的企业,预计上市后能更好地满足临床需求。
地拉罗司分散片被列入第一批鼓励仿制药目录,奥赛康成功获得中国第一批仿制药目录。
表4:奥赛康报生产并在审
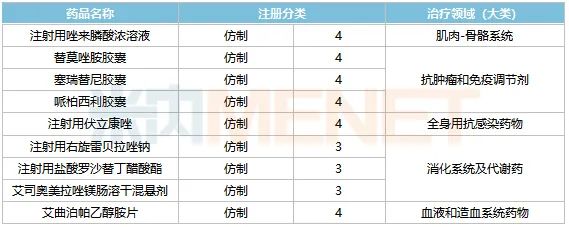
来源:米内网MED2.中国药品评价数据库
目前,奥赛康还有9种高端仿制药报产并在审,涉及五大类,其中4种有望影响国内首仿。
抗肿瘤和免疫调节剂将有三种口服制剂需要批准,其中塞瑞替尼胶囊为ALK、胰岛素样生长因子1(IGF-1R)、胰岛素受体(INSR)和ROS1等多靶激酶抑制剂,原制药公司诺华于2018年获批进入中国市场,谈判成功进入国家医疗保险目录,2020年在中国公立医疗机构终端销售超过2种.6亿元。奥赛康表示,公司是第一家完成生物等效性试验的企业,并于2021年2月首家报产,抢占国内首仿具有较大的时间优势。
作为国内PPI制剂龙头企业奥赛康也将有两个重磅第一模仿即将到来。右旋雷贝拉唑钠是雷贝拉唑钠的右旋反映异构体,疗效更好,剂量更少,半衰期更长。2018年,奥赛康提交了注射用右旋雷贝拉唑钠三类仿制上市申请。目前,只有一家企业在审批中获得了国内第一批仿制品。此外,艾司奥美拉唑镁肠溶干混悬剂是FDA唯一获准用于儿科患者的PPI制剂已被列入第二批鼓励儿童药品研发申报清单。目前,中国已有4家企业申请上市,但尚未获批,奥赛康仍有机会扭转局面。与此同时,等待这两个重磅PPI新产品获批后,将进一步提升公司在该领域的领导地位。
此外,在血液和造血系统药物领域,奥赛康也是第一家完成生物等效性试验并申请生产的企业。作为第一种治疗方法ITP(原发免疫性血小板减少症)口服药物给药更方便,患者依从性高,可显著降低出血率。目前,中国只有诺华获批进口,2020年中国公立医疗机构终端销售额为1.8亿元左右,现为2021全国医疗保险谈判目录品种。目前,除奥赛康外,还有正大天晴药业集团、齐鲁制药、四川科伦等国内明星制药企业报批。该产品的第一次模仿之争非常激烈。
从待批上市的高端仿制药情况来看,奥赛康正在不断巩固据领先地位的地位PPI制剂市场,同时,为了与一类新药协调发展,在抗肿瘤、免疫调节剂、全身抗感染药物两大市场攻击第一仿制品和重品种,也印证了公司向创新药为主,高端第一仿制品为辅的产品转型升级战略。
第七批国采如约而至,50亿大品种激战展开
近日,第七批国采正式正式宣布,58个品种和208个品种即将展开市场竞争。奥赛康积极参与第四批、第五批国采,共中标注射帕瑞昔布钠、注射潘托拉唑钠、多西他赛注射液、注射地西他滨、沙格列汀片、盐酸帕洛诺司琼注射液、注射艾司奥美拉唑钠、注射兰索拉唑8种产品。
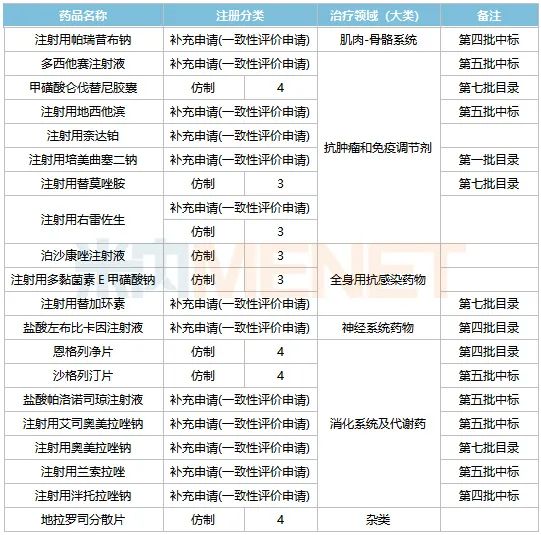
到目前为止,奥赛康已经评估了20种产品,其中包括甲磺酸仑伐替尼胶囊、替莫唑胺、替加环素和奥美拉唑钠。
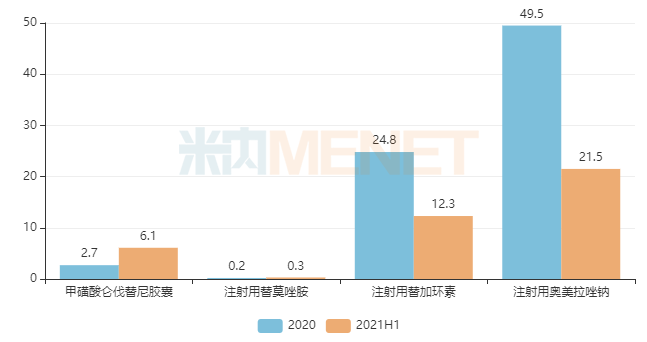
甲磺酸仑伐替尼胶囊原研制药公司材,2018年获批进入中国市场,2020年进入国家医保谈判目录后销量飙升,2021年上半年已超过6亿元。2021年7月,国内仿制药开始陆续获批上市。截至目前,奥赛康、石药欧意、湖南科伦、齐鲁等8家国内药企已按新分类获批,均在同一起跑线上。
恒瑞于2018年首次获得注射用替莫唑胺生产批准。目前,该产品由恒瑞领先。2021年,奥赛康等3家国内制药企业参与市场竞争。上半年销售增长率高达414%,市场潜力迅速释放。
注射用替加环素是全身用抗细菌药物超过20亿大品种,2021年上半年豪森用360亿元.54%的市场份额领先市场,辉瑞排名第二(24%.奥赛康排名第六(24%).78%),截至目前,该产品已有7家过评企业。
第三批国采时纳入奥美拉唑肠溶胶囊,海南海灵、山东罗新药业集团成功中标。2019年,上述中标企业市场份额分别为0.02%、11.2021年上半年,19%上升到8%.59%、18.60%,两家中标企业以价换量取得巨大成功。第七批国采专注于奥美拉唑注射剂,目前只有奥美拉唑钠注射过评价,但多达24家企业。
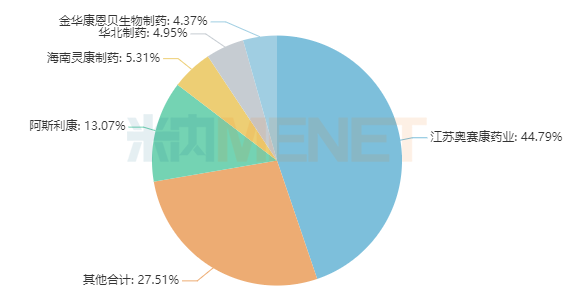
2021年上半年在中国公立医疗机构终端注射奥美拉唑钠的龙头企业为奥赛康,阿斯利康仅为13家.07%,紧随其后的灵康制药、华北制药和康恩贝也受到了批评。作为公司的拳头产品,奥赛康有望全力以赴,但同时可以预见,这场近50亿元的重量级注射剂激战已不可避免。
