IL-4R度普利尤单抗:全球销售额60亿美元!
发布时间: 2022-03-10 10:37:50
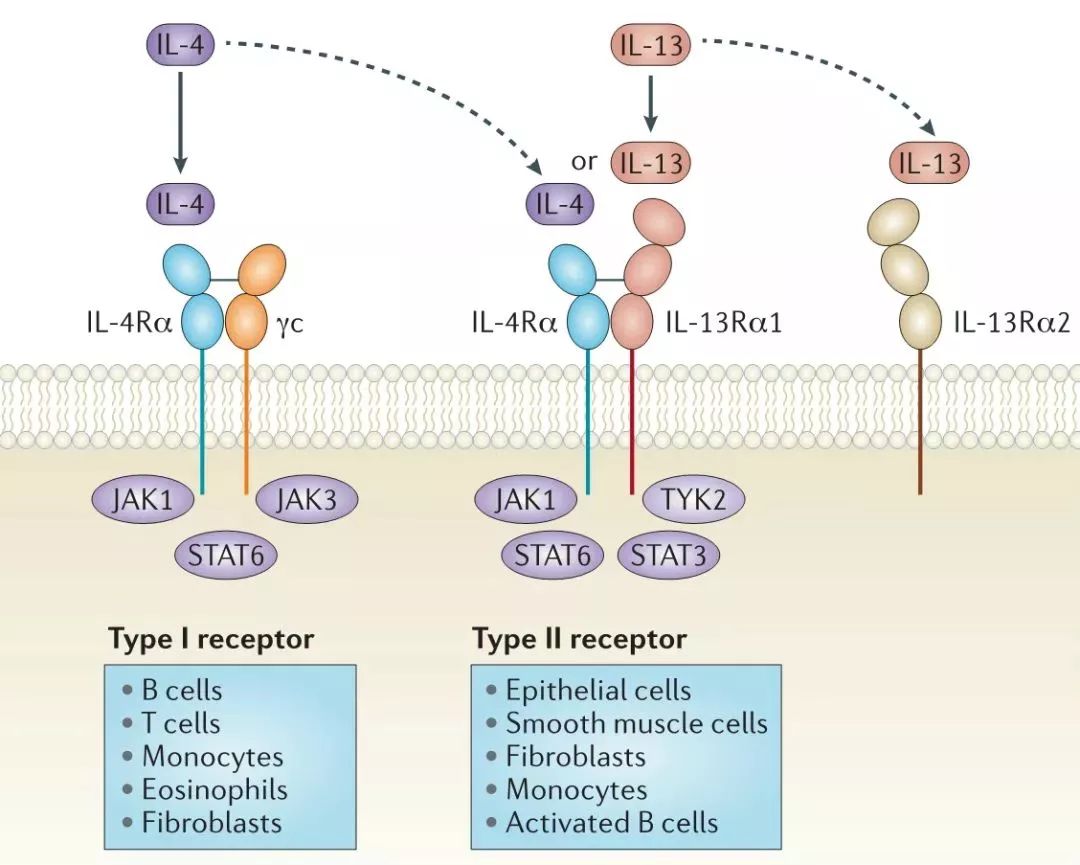
度普利尤单抗(Dupilumab注射液)由再生元组成(Regeneron)与赛诺菲开发的全人单克隆抗体是针对赛诺菲的IL-4Rα上同时结合IL-4及IL-13因此,亚基可以同时阻断IL-4及IL-13信号传输。
度普利特单抗注射液基本信息

截图来源:药融云全球药物研发数据库
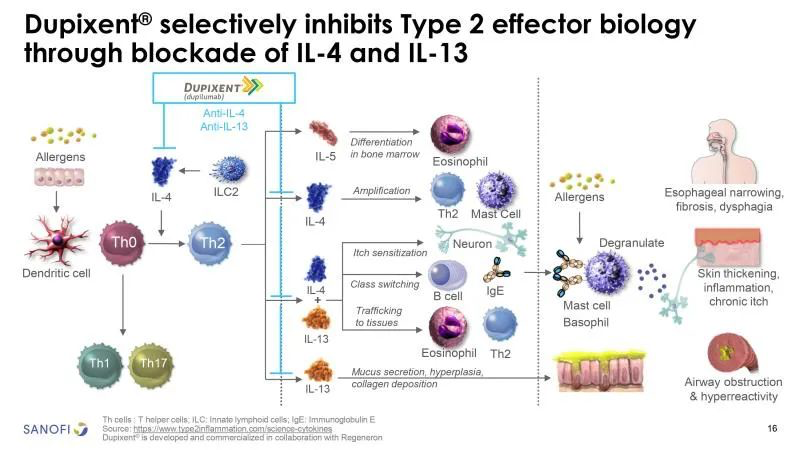
2017 3月 28日,度普利尤单抗击美国 FDA 批准上市,成为治疗中重度特应性皮炎的第一种生物制剂。目前批准的适应症有:中重度特应性皮炎(AD)、哮喘,慢性鼻-鼻窦炎伴鼻息肉(CRSwNP)、6-11中重度哮喘、中重度哮喘、中重度哮喘、中重度哮喘6-11中重度特应性皮炎等。
根据赛诺菲年报/季报,度普利尤单抗(Dupilumab注射液)2018年销售收入达到7.882019年达到1亿欧元;20.74欧元(约合22.491亿美元),同比增长152%。2020年全球销售额为35.342021年全球销售额达到1亿欧元。52.49亿欧元;同比增长48.53%。
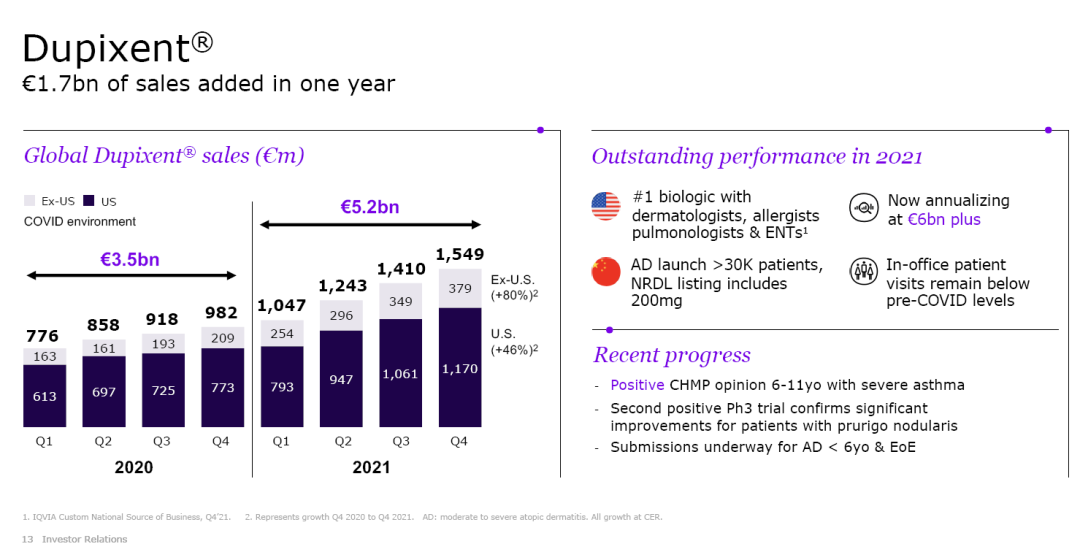
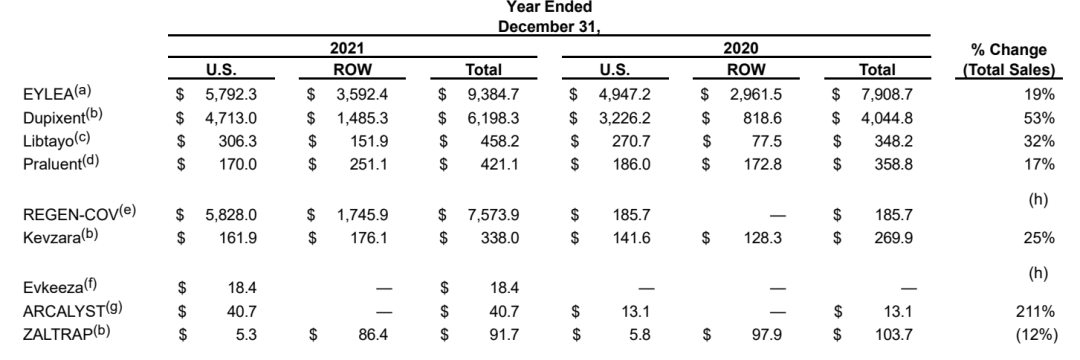
▲赛诺菲(上图)与再生元(下图)的统计表现略有差异,可能是权益合作、汇率等因素造成的。
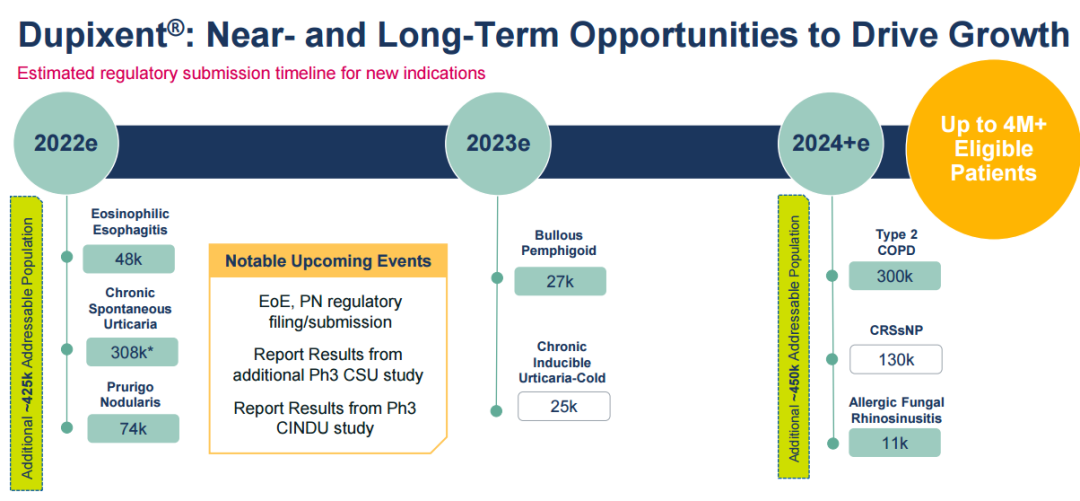
再生元/赛诺菲对度普利尤单抗(Dupilumab注射液)寄予厚望,预计销售峰值将超过100亿欧元,成为超级重型炸弹,基于许多关键临床积极进行(结节性瘙痒疹、嗜酸性粒细胞性食管炎等)。
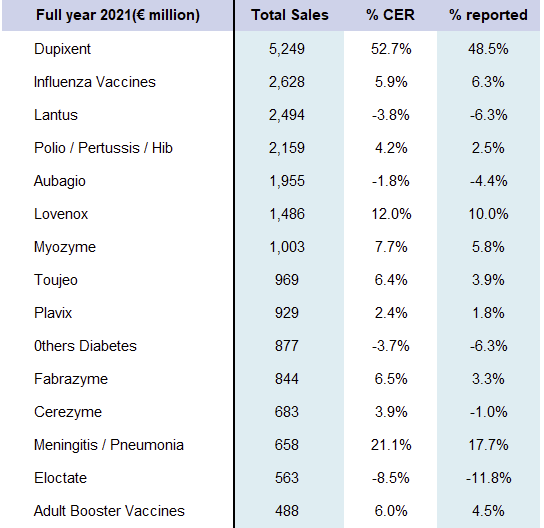
▲赛诺菲2021财年主要产品业绩
度普利尤单抗中国
20206月在度普利特单抗性(Dupilumab注射液)中国批准成人中重度特应性皮炎适应症,注册证号:S20200017。20202012年12月底,经国家医疗保险谈判,正式列入国家基本医疗保险、工伤保险和生育保险药品目录(2020年),是新医疗保险目录中唯一治疗中重度特应性皮炎的靶向生物制剂,用于传统治疗无效、禁忌或不耐受的中重度特应性皮炎。度普利尤单抗上市仅5个月就被列入国家医疗保险目录,值得国内制药公司关注;公司将大幅降价。
20212009年9月,度普利尤单抗注射液被批准治疗12岁以上青少年和成人中重度特应性皮炎,用于治疗外用药物控制不良或不建议使用外用药物。赛诺菲仍是该药品的独家制药公司,国内没有制药公司报告生产该仿制药。
度普利特单抗注射液中国批文信息
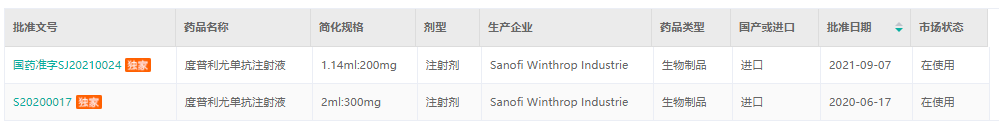
截图来源:药云中国药品批文数据库
20222月,中国国家药品监督管理局获得度普利特单抗注射液(NMPA)批准扩大6岁以上儿童和成人中重度特应性皮炎,用于治疗外用药物控制不良或不建议使用外用药物。儿童新适应症的批准是基于一项关键的全球儿童三期临床试验,以及中国成人和青少年中重度特应性皮炎适应症的数据。这是一项随机、双盲、安慰剂对照研究,评估了当地外用皮质类固醇(杜普利特单抗注射)(TCS)治疗儿童严重特应性皮炎的疗效和安全性。在实验中,接受达必妥和和和。TCS联合治疗儿童患者的整体病情严重程度、皮肤清除率和瘙痒程度较高TCS单个药组都有了显著的改善。数据显示,达必妥和和和。TCS联合治疗组中皮损清除或几乎清除的患者人数达到TCS单药组的两倍多,瘙痒程度明显缓解的患者数量是TCS单药组的4倍以上,患者总体改善程度至少75%,平均改善程度约80%。
湿疹难耐
特应性皮炎(atopic dermatitis,AD)(湿疹,eczema)是一种慢性、复发、炎症性皮肤病,患者常有严重瘙痒,严重影响生活质量。AD它是最常见的皮肤病之一,影响20%的儿童和1-3成年人的%。
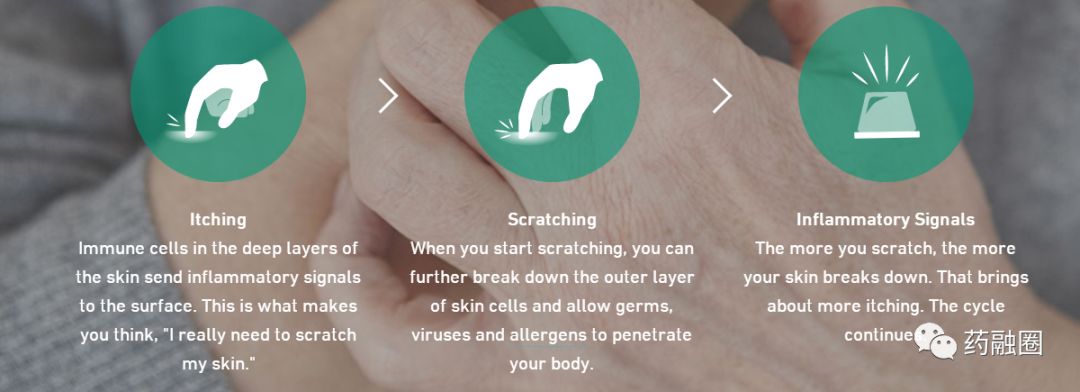
超过一半的病人去了医院,主要症状是大面积皮疹和难以忍受的严重瘙痒。患者生活质量低下,常伴有睡眠障碍、焦虑、抑郁等精神疾病,严重影响患者的学习、工作和社会活动。对于中重度特应性皮炎患者,现有的药物治疗方法非常有限,临床急需安全、有效、长期使用的全身治疗方法。
新药在研
Th2通道在自身免疫疾病中起着重要作用。多种类型。IL-4、IL-5、IL-13抗体新药相继获批。全球范围内有:Dupilumab(IL-4R)、Mepolizumab(IL-5)、Benralizumab(IL-5R)、Reslizumab(IL-5)。
经药融云数据查询,全球共有2款IL-4R除了赛诺菲的度普利尤单抗,还有一种靶点生物药品获批上市。Actimmune,来自Clinigen Group和Horizon Therapeutics。国内布局IL-4R靶点生物药物Biotech超过10家:洛奇生物(单域抗体)(CM310)、康乃德(CBP-201)、康方生物(AK120)、荃信生物(QX005)、三生国健(公司研发代号:611)(TS0001)等等。
IL-4R靶点生物药全球研发阶段
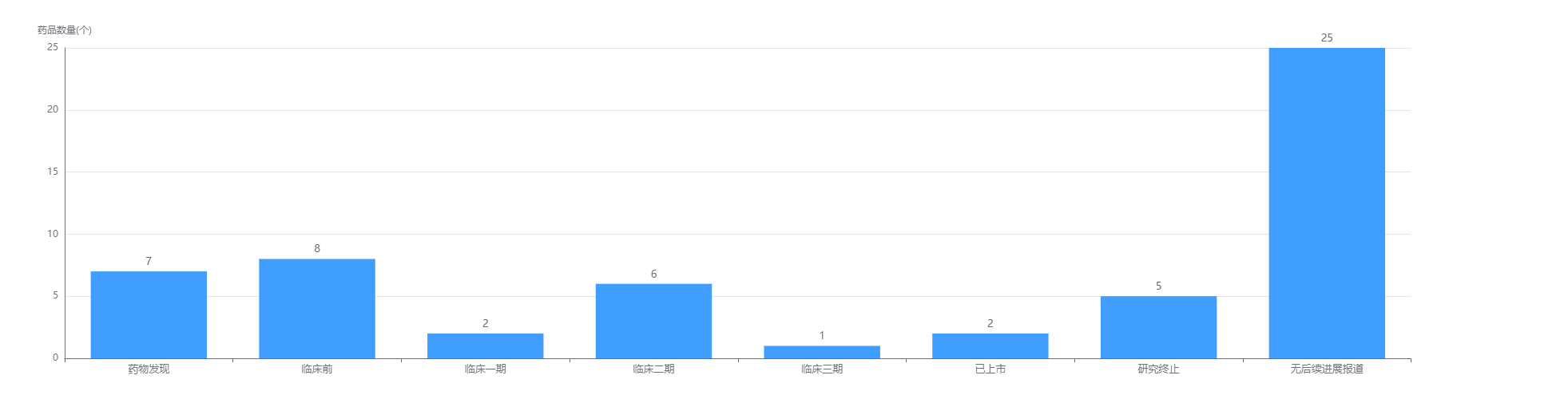
截图来源:药融云全球药物研发数据库
IL-4R国内布局靶点生物药
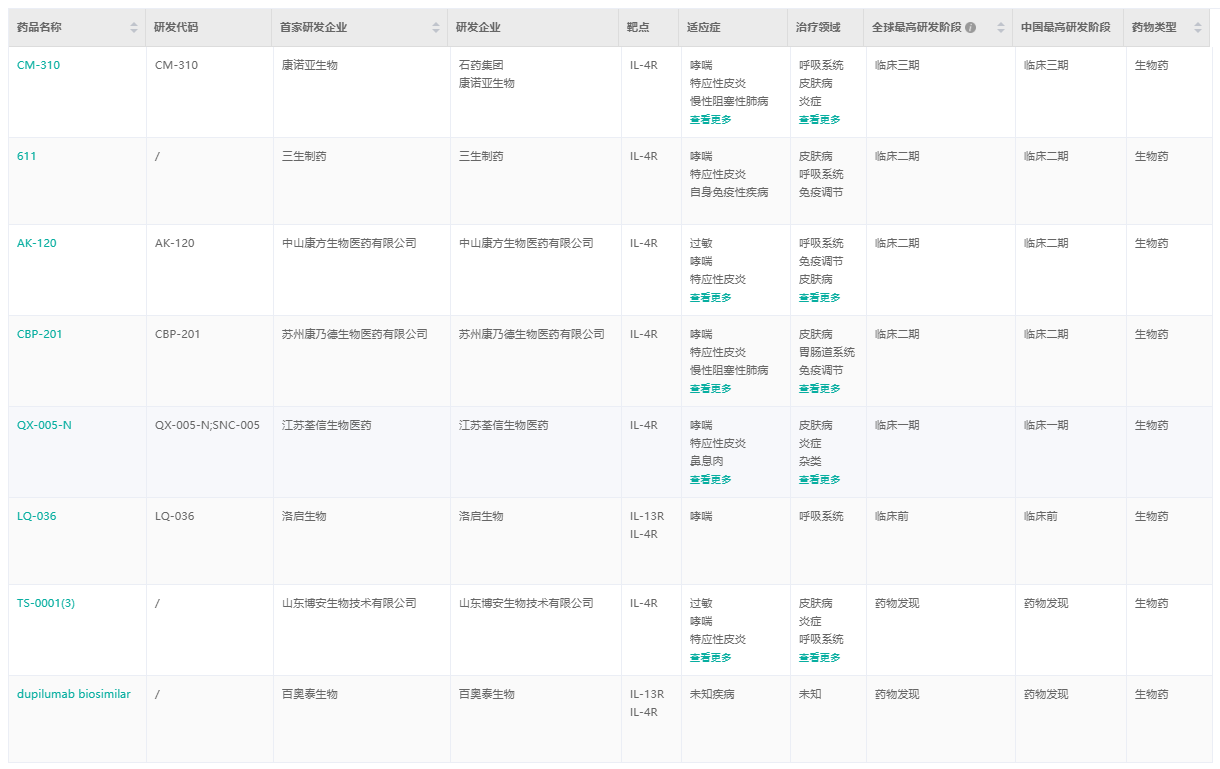
截图来源:药融云全球药物研发数据库
