Harpoon宣布HPN217获美国FDA授予快速通道资格
发布时间: 2022-03-07 10:37:23
日前,Harpoon Therapeutics公司宣布,美国FDA已授予HPN217快速通道资格用于治疗已接受至少四线治疗的复发/难治性多发性骨髓瘤患者。这是一个靶向的目标。B细胞成熟抗原(BCMA)的三特异性T细胞激活疗法。目前,该药物正在进行1/2的临床试验,以评估其疗效和安全性。
Harpoon开发的新型T细胞衔接器(T Cell engagers)利用人体免疫系统的力量治疗癌症等疾病。T细胞连接器是一种利用生物工程改造的蛋白质,可以引导患者自身T细胞杀死靶细胞。它们的一端胞表面抗原结合,另一端与靶细胞表面抗原结合。T刺激细胞表面受体结合,刺激细胞表面受体T细胞杀死靶细胞。这种免疫治疗与靶细胞相似。CAR-T,但分子量较小,人体半衰期较短。决这个问题,Harpoon利用其专有技术平台开发新型三特异性T细胞连接器,通过与血液中的白蛋白结合,可以延长人体内药物的半衰期,带来更好的治疗效果。
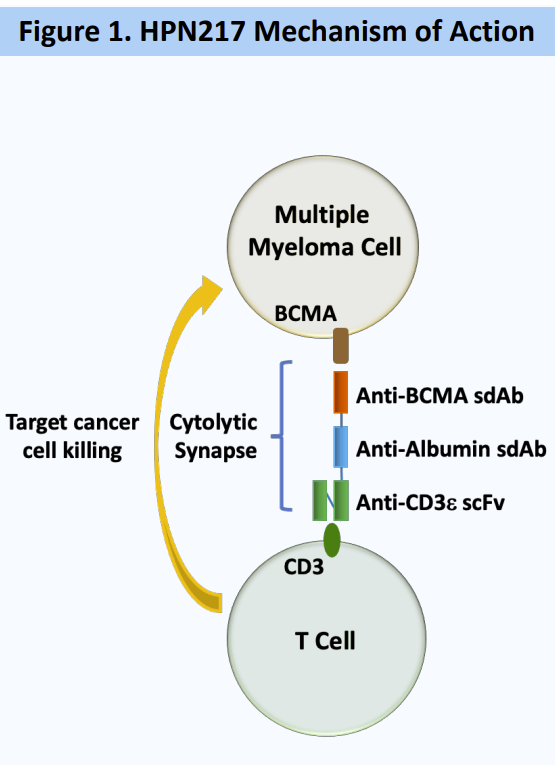
HPN217是靶向BCMA阳性肿瘤细胞T细胞连接器,可以筹集病人T细胞,杀伤BCMA阳性肿瘤细胞。临床前数据显示,HPN217基于细胞培养和异种移植动物模型BCMA和T细胞的抗肿瘤活性。药代动力学研究表明,HPN217动物体内的半衰期是70-84一个小时。重要的是,在血液循环中存在一周后,HPN217功能仍然完整。
此外,新闻稿还提到,2019年11月,Harpoon和艾伯维(AbbVie)根据协议条款,艾伯维可以在完成1/2期临床试验后行使获得许可协议。HPN217许可的选择权。
(原文删除)
