消化道癌症热门靶点Claudin 18.2 |全球临床管道盘点
59月9日,科济药业靶向CLDN18.2(Claudin18.2)的CAR-T细胞候选产品CT0411期中分析结果发表在Nature Medicine上,CT041为适应症CLDN18.2目前,已经开始了第二阶段的消化道阳性肿瘤确认性临床试验。这一最新临床试验数据的发布也引起了业界的高度关注。CLDN18.2是近年来治疗实体瘤的热门目标。在本文中,药明康德内容团队将介绍有关这一目标的信息和研究管道。
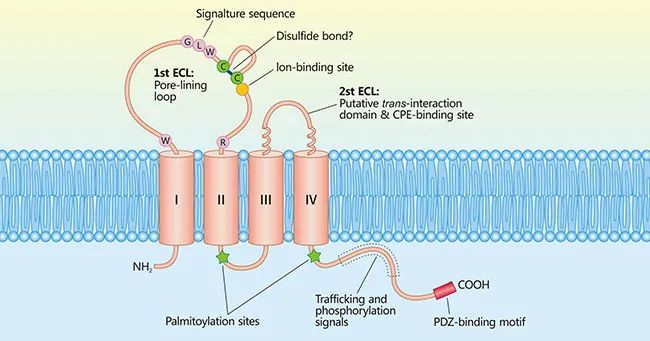
▲Claudin蛋白质结构(图片来源:参考资料[8])
揭秘CLDN18.2:对抗实体瘤新宠
CLDN(Claudin)它是一种重要的蛋白质,在正常组织的紧密连接中,有四个跨膜结构域,CLDN其功能是参与细胞旁通性和电导过程的调节。1998年,日本科学家Shoichiro Tsukita博士和他的同事第一次发现CLDN。CLDN家族包括至少27名成员,包括CLDN18有CLDN18.1和CLDN18.2两种异构体。
2008年,Ganymed公司创始人和癌症免疫治疗专家Ugur Sahin医生和其他人发现,在正常的生理状态下,CLDN18.2它仅表达在胃粘膜上分化的上皮细胞中,而不表达在其他健康组织中。然而,在许多肿瘤中,如胃癌、食管癌、胰腺癌、肺癌、卵巢癌和结肠癌,CLDN18.2但是表现出高表现象。CLDN18.2有可能成为胃癌、胰腺癌等实体肿瘤免疫治疗的有效目标。
虽然CLDN18.2实体瘤靶向疗法的发展具有潜力,但这一领域的发展进展相对缓慢。2016年,Ganymed在美国临床肿瘤学会(ASCO)宣布年会CLDN18.2靶向单抗zolbetuximab的2b临床试验结果以黑马的姿态成为当年ASCO年会最大的亮点之一。CLDN18.2这一抗癌目标也引起了业界的广泛关注。安斯泰来当年以14亿美元的收购价格Ganymed该公司获得了其核心资产zolbetuximab(曾用名:IMAB362),zolbetuximab这也是世界上第一个进入三期临床研究的靶向研究CLDN18.2治疗。值得一提的是,Ugur Sahin博士夫妇也是如此BioNTech公司的创始人。
自CLDN18.2在引起关注后,许多公司争相瞄准CLDN18.2药品布局。总的来说,大多数CLDN18.2目标药物仍处于早期开发阶段。
临床阶段在研治疗概述:多种治疗模式
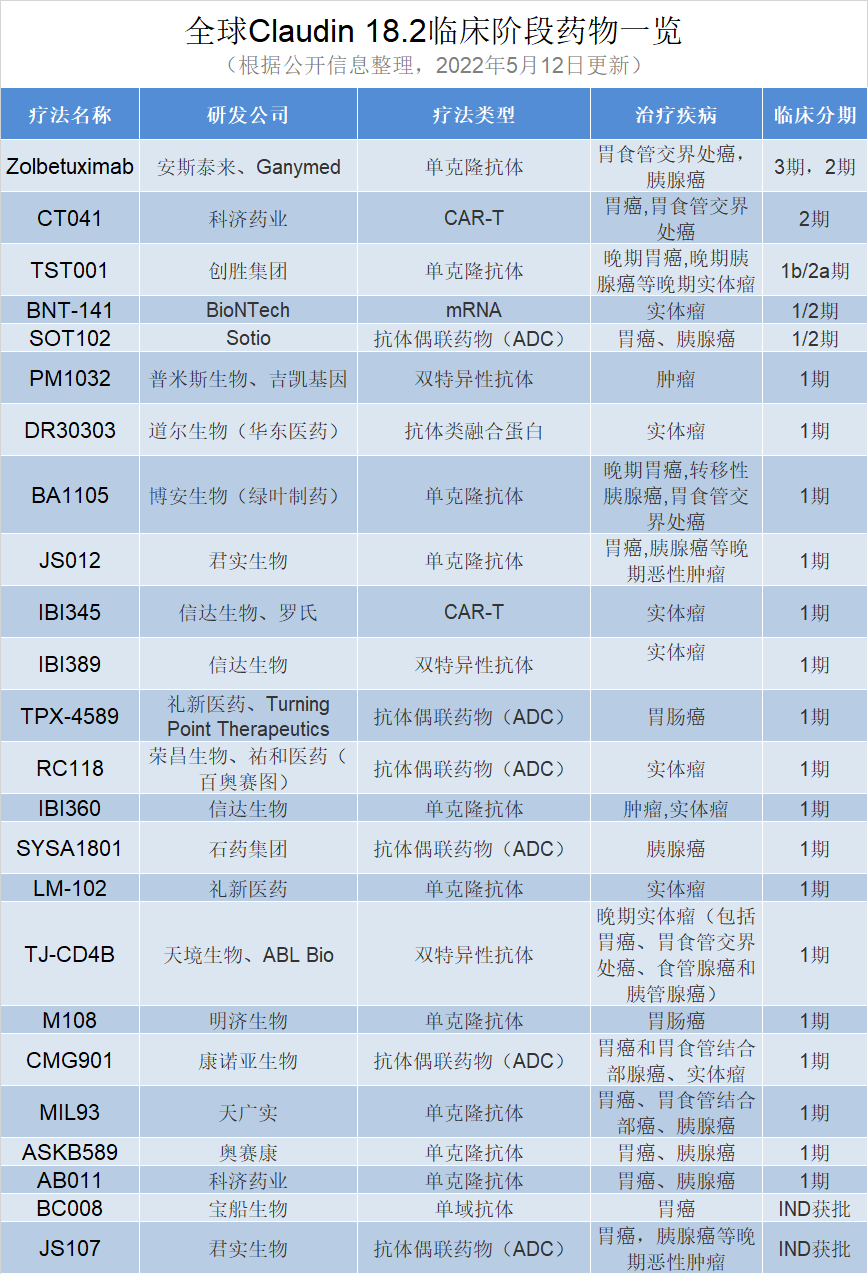
据不完全统计,目前全球共有24款靶向车型CLDN18.2治疗正处于临床发展阶段(包括2个模型)IND申请批准的疗法)。
其中,有两种疗法已经进入二期和三期临床阶段,即安斯泰来zolbetuximab还有科济药业CT-041。
有三种疗法处于1/2期的临床阶段,创胜者TST001、BioNTech的BNT-141和Sotio的SOT102。
17这种疗法正在进行第一阶段的临床试验。值得注意的是,这些疗法大部分是由中国公司开发的。信达生物、礼新药、君实生物等多种药物上榜,可见中国制药企业CLDN18.2这个目标的积极布局。此外,礼新药最近将以2500万美元的首付和10多亿美元的潜在总额支付新药LM-302授权在大中华区和韩国以外的全球开发和商业化权益Turning Point Therapeutics。
针对热门靶点CLDN18.2临床疗法在研究中取得的进展备受关注。接下来,我们将首先从两种治疗方法开始,临床进展很快。zolbetuximab和CT-041说起。
Zolbetuximab是一种IgG1单克隆抗体,在肿瘤细胞表面和CLDN18.2特异性结合导致抗体依赖细胞毒性(ADCC)、补充依赖细胞毒性(CDC),肿瘤细胞增殖的凋亡和抑制。
Zolbetuximab在二期临床试验中与一线化疗联合可以改善CLDN18.2无进展生存期和总生存期的患者(OS)。目前,这种治疗方法正在进行三期临床试验,以评估其对性CLDN18.2胃和食管胃结合腺癌患者阳性、转移性或晚期无法切除。此外,评估zolbetuximab结合白蛋白组合紫杉醇和吉西他滨CLDN18.2研究阳性转移性胰腺癌患者的疗效和安全性。
CT041是一款靶向CLDN18.2的自体CAR-T细胞候选产品。CT041已经获得FDA再生医学先进疗法(RMAT)资格,用于治疗CLDN18.2晚期胃癌/食管胃结合腺癌阳性;获得欧洲药品管理局(EMA)给予优先药物(PRIME)治疗晚期胃癌的资格。
本文开头提到的发表Nature Medicine上述研究是在中国开展的一期临床试验,多中心,开放标签,评估CT041治疗CLDN18.2晚期消化系统肿瘤阳性患者的安全性、有效性和细胞代谢动力学。结果显示,在37例晚期消化系统肿瘤患者中,CT041整体耐受性好,安全风险可控。CT041消化系统肿瘤患者的客观缓解率(ORR)以及疾病控制率(DCR)分别为48.6%和73.0在胃癌患者中,%ORR和DCR分别达到57.1%和75.0%。
针对CT041,科济制药在中国对晚期胃癌/食管胃结合腺癌和胰腺癌进行了临床试验1b晚期胃癌/食管胃结合腺癌2期临床试验和晚期胃癌或胰腺癌2期临床试验在北美启动1b计划今年在北美启动关键二期临床试验。
1期和22款IND临床治疗药物中,单克隆抗体数量最多,有9种;第二种是抗体偶联药,有6种。同时,也有特殊类型,如mRNA、CAR-T细胞疗法、单域抗体和融合蛋白的出现。适应症集中在胃、胰腺等消化道实体肿瘤,其中胃癌药物11种,胰腺癌药物10种。
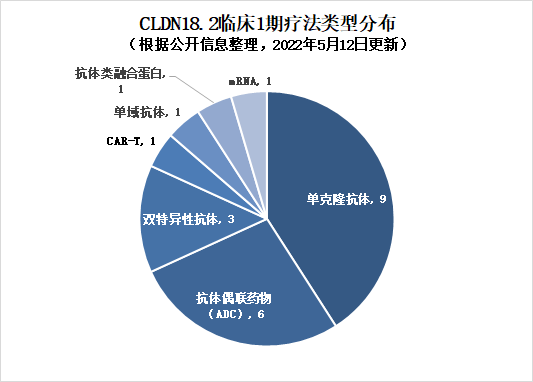
▲CLDN18.2临床一期治疗类型分布(药明康德内容团队制图,点击可见大图)
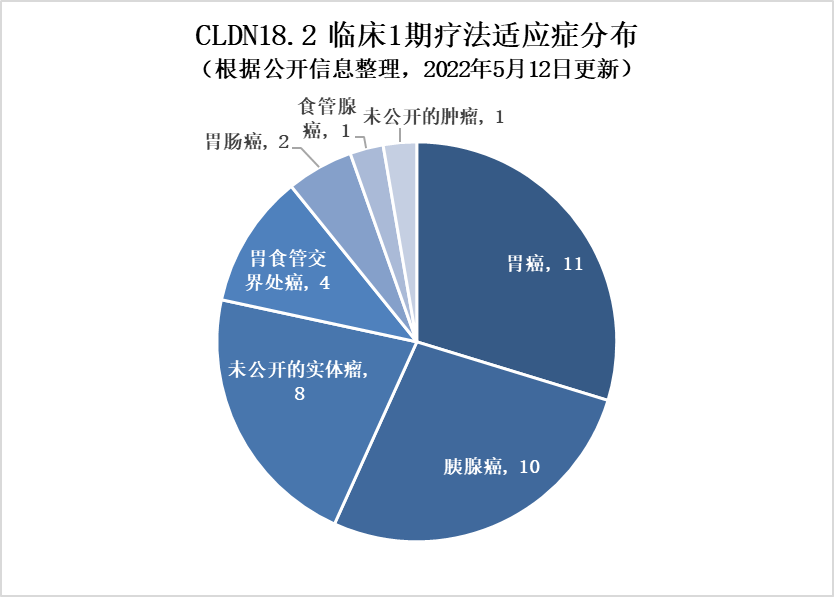
▲CLDN18.2临床一期治疗适应症分布(药明康德内容团队制图,点击可见大图)
有三种疗法已经进入临床1/2期,分别是创胜集团的单克隆抗体TST001,BioNTech的mRNA疗法BNT-141以及Sotio抗体偶联药物SOT102。其中,值得一提的是,它是目前世界上唯一潜在的管道mRNA疗法,BioTech的BNT-141用核苷修饰mRNA设计用于减少免疫原性,避免免疫反应,并可在细胞中翻译成靶向CLDN18.2抗体。这种疗法使用脂质纳米颗粒靶向肝脏(LNP)采用静脉给药技术,保证抗体的全身可用性,延长编码抗体在体内的作用时间。
参考资料:
[1]重磅| 科济药业CT041研究人员开始实验CAR-T细胞治疗消化系统肿瘤的研究结果《Nature Medicine》杂志发表. Retrieved May 10,2022. from https://mp.weixin.qq.com/s/el8Miuc3_k58JutalJeXaQ
[2] Furuse et al.,(1998). Claudin-1 and -2: Novel Integral Membrane Proteins Localizing at Tight Junctions with No Sequence Similarity to Occludin. Journal of Cell Biology,https://doi.org/10.1083/jcb.141.7.1539
[3] Sanada et al.,(2006). Down-regulation of the claudin-18 gene,identified through serial analysis of gene expression data analysis,in gastric cancer with an intestinal phenotype. The Journal of Pathology,https://doi: 10.1002/path.1922
[4] Singh et al.,(2017). Anti-claudin 18.2 antibody as new targeted therapy for advanced gastric cancer. Journal of Hematology
